Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

PTHH ( I ) : \(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\) .
PTHH ( II ) : \(ZnO+2HCl\rightarrow ZnCl_2+H_2O\) .
\(n_{H_2}=\frac{V_{H_2}}{22,4}=\frac{4,48}{22,4}=0,2\left(mol\right)\)
- Theo PTHH ( I ) : \(n_{Zn}=n_{ZnCl_2}=n_{H_2}=0,2\left(mol\right)\)
=> \(m_{Zn}=n.M=0,2.65=13\left(g\right)\)
=> \(m_{ZnCl_2}=n.M=0,2.\left(65+35,5.2\right)=27,2\left(g\right)\)
Mà sau phản ứng chỉ thu được \(ZnCl_2\) .
=> mmuối khan \(=m_{ZnCl_2\left(I\right)}+m_{ZnCl_2\left(II\right)}=27,2+m_{ZnCl_2\left(II\right)}=40,8\)
=> \(m_{ZnCl_2\left(II\right)}=13,6\left(g\right)\)
=> \(n_{ZnCl2}=\frac{m}{M}=\frac{13,6}{65+35,5.2}=0,1\left(mol\right)\)
Theo PTHH ( II ) : \(n_{ZnO}=n_{ZnCl_2}=0,1\left(mol\right)\)
=> \(m_{ZnO}=n.M=0,1.\left(16+65\right)=8,1\left(g\right)\)

Đáp án B
mNaOH = v.d.C% = 31,25.1,12.16% = 5,6 (gam)
Þ nNaOH = 0,14
Các phản ứng xảy ra theo thứ tự:
2NaOH + H2SO4 g Na2SO4 + 2H2O
Cu(NO3)2 + 2NaOH g Cu(OH)2¯ + 2NaNO3
Cu(OH)2 g CuO + H2O
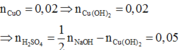
Do đó trong 50ml dung dịch B chứa 0,05 mol H2SO4 và 0,02 mol Cu(NO3)2 .
Khi cho 50ml dung dịch B tác dụng với 0,0375 mol Cu thì:
3Cu+4H2SO4+Cu(NO3)2g4CuSO4+2NO+4H2O
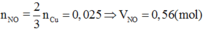

Đáp án B
mNaOH = v.d.C% = 31,25.1,12.16% = 5,6 (gam)
Þ nNaOH = 0,14
Các phản ứng xảy ra theo thứ tự:
2NaOH + H2SO4 g Na2SO4 + 2H2O
Cu(NO3)2 + 2NaOH g Cu(OH)2¯ + 2NaNO3
Cu(OH)2 g CuO + H2O
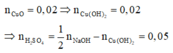
Do đó trong 50ml dung dịch B chứa 0,05 mol H2SO4 và 0,02 mol Cu(NO3)2 .
Khi cho 50ml dung dịch B tác dụng với 0,0375 mol Cu thì:
3Cu+4H2SO4+Cu(NO3)2g4CuSO4+2NO+4H2O
Do đó
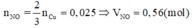

2KMnO4--->K2MnO4+MNO2+O2
3O2+4Al---2Al2O3
a) m O2=m KMNO4-m chất rắn=16-12=4(g)
n O2=4/16=0,25(mol)
V O2=0,25.22,4=5,6(l)
b) n Al=5,4/27=0,2(mol)
-->O2 dư
n Al2O3=1/2n Al=0,1(mol)
m Al2O3=0,1.102=10,2(g)
c) n O2=3/4n Al=0,15(mol)
n O2 dư=0,25-0,15=0,1(mol)
m O2 dư=0,1.32=3,2(g)

a, 2KNO3 ----> 2KNO2 + O2
n KNO3= m/M= 60.6/101= 0.6 mol
n KNO3=1/2 n O2 => n O2= 0.6/2= 0.3 mol
b,V O2= n . 22.4 = 0.3 . 22.4 = 6.72 l
n Al= m/M= 13.5/27= 0.5 mol
4Al + 3O2 ----> 2Al2O3
Xét n Al : n O2 = n Al đề bài/ n Al phương trình : n O2 đề bài/ O2 phương trình= 0.5/4 : 0.3/3 = 0.125 > 0.1
=> O2 hết Al dư. Sản phẩm tính theo O2
=> n Al2O3= (0.3 .2)/3= 0.2 mol
Chất rắn thu được ngoài Al2O3 còn có Al dư.
n Al dư= 0.5-[(0.3 .4)/3] = 0.1 mol
=> m Al2O3= n.M= 0.2 . 102=20.4 g
m Al dư= n Al dư . M= 0.1 . 27= 2.7 g