Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nMg = 7,2/24 = 0,3 (mol)
PTHH: Mg + 2HCl -> MgCl2 + H2
Mol: 0,3 ---> 0,6 ---> 0,3 ---> 0,3
VH2 = 0,3 . 22,4 = 6,72 (l)
nFe = 19,2/160 = 0,12 (mol)
PTHH: Fe2O3 + 3H2 -> (t°) 2Fe + 3H2O
LTL: 0,12 > 0,3/3 => Fe2O3 dư
nFe = 0,3 : 3 . 2 = 0,2 (mol)
mFe = 0,2.56 = 11,2 (g)
\(n_{Mg}=\dfrac{7,2}{24}=0,3\left(mol\right)\)
PTHH: \(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\)
1 2 1 1
0,3 0,6 0,3 0,3
a/ \(V_{H_2\left(đktc\right)}=n.22,4=0,3.22,4=6.72\left(l\right)\)
b/ \(n_{Fe_2O_3}=\dfrac{19,2}{160}=0,12\left(mol\right)\)
PTHH: \(Fe_2O_3+3H_2\rightarrow2Fe+3H_2O\)
1 3 2 3
0,12 0,3
-Chuyển thành tỉ lệ: \(\dfrac{0,12}{1}>\dfrac{0,3}{3}\)
\(\Rightarrow\)H2 phản ứng hết còn Fe2O3 dư.
-Theo PTHH trên: \(n_{Fe}=\dfrac{0,3.2}{3}=0,2\left(mol\right)\)
\(\Rightarrow m_{Fe}=n.M=0,2.56=11,2\left(g\right)\)

\(n_{Zn}=\dfrac{19,5}{65}=0,3\left(mol\right)\\ PTHH:Zn+2HCl\rightarrow ZnCl_2+H_2\\ n_{H_2}=n_{Zn}=0,3\left(mol\right)\\ a,V_{H_2\left(đktc\right)}=0,3.22,4=6,72\left(l\right)\\ b,n_{Fe_2O_3}=\dfrac{19,2}{160}=0,12\left(mol\right)\\ PTHH:3H_2+Fe_2O_3\rightarrow\left(t^o\right)2Fe+3H_2O\\ Vì:\dfrac{0,3}{3}< \dfrac{0,12}{1}\Rightarrow Fe_2O_3dư,H_2.hết\\ n_{Fe}=\dfrac{2}{3}.n_{H_2}=\dfrac{2}{3}.0,3=0,2\left(mol\right)\\ m_{Fe}=0,2.56=11,2\left(g\right)\)

a) số mol của 19,5 gam Zn:
\(n_{Zn}=\dfrac{m}{M}=\dfrac{19,5}{65}=0,3\left(mol\right)\)
PTHH: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\uparrow\)
Tỉ lệ : 1 : 1 : 1 : 1
0,3-> 0,3 : 0,3 : 0,3
thể tích của 0,3 mol H2:
\(V_{H_2}=n.22,4=0,3.22,4=6,72\left(l\right)\)
b) số mol của 19,2 gam Fe2O3:
\(n_{Fe_2O_3}=\dfrac{m}{M}=\dfrac{19,2}{160}=0,12\left(mol\right)\)
PTHH:
\(3H_2+Fe_2O_3\underrightarrow{t^o}2Fe+3H_2O\)
3 : 1 : 2 : 3
0,12-> 0,04 : 0,08 : 0,12 (mol)
Khối lượng của 0,08 mol Fe:
\(m_{Fe}=n.M=0,08.56=4,48\left(g\right)\)
PTHH: Zn + 2HCl ---> ZnCl₂ + H₂
1 2 1 1 ( mol)
a):Số mol Zn: nZn = 19,5 ÷ 65 = 0,3 mol.
Theo PTHH => Số mol H₂: nH₂ = 0,3 × 1 ÷ 1 = 0,3 mol
=> Thể tích H₂ (đktc): V = n × 22,4 = 0,3 × 22,4 = 6,72 lít
b) PTHH: Fe₂O₃ + 3H₂ --> 2Fe + 3H₂O
1 3 2 3 (mol)
*Lm tương tự nhưng thay vì tính thể tích thì tính KL Fe

nZn = 19.5/65 = 0.3 (mol)
Zn + 2HCl => ZnCl2 + H2
0.3................................0.3
VH2 = 0.3 * 22.4 = 6.72 (l)
nFe2O3 = 19.2/160 = 0.12 (mol)
Fe2O3 + 3H2 -t0-> 2Fe + 3H2O
Bđ: 0.12......0.3
Pư: 0.1........0.3..........0.2
Kt: 0.02.........0...........0.2
mFe = 0.2 * 56 = 11.2 (g)

\(n_{Zn}=\dfrac{19,5}{65}=0,3\left(mol\right)\\
pthh:Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,3 0,3
\(V_{H_2}=0,3.22,4=6,72l\\ n_{Fe_2O_3}=\dfrac{19,2}{160}=0,12g\\ pthh:Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\\ LTL:\dfrac{0,12}{1}>\dfrac{0,3}{3}\)
=> Fe2O3 dư
\(n_{Fe}=\dfrac{2}{3}n_{H_2}=0,2\left(mol\right)\\
m_{Fe}=0,2.56=11,2g\)
a.\(n_{Zn}=\dfrac{19,5}{65}=0,3mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,3 0,3 ( mol )
\(V_{H_2}=0,3.22,4=6,72l\)
b.\(n_{Fe_2O_3}=\dfrac{19,2}{160}=0,12mol\)
\(Fe_2O_3+3H_2\rightarrow\left(t^o\right)2Fe+3H_2O\)
0,12 > 0,3 ( mol )
0,3 0,2 ( mol )
\(m_{Fe}=0,2.56=11,2g\)

Giải thích các bước giải:
a) Mg +H2SO4--->MGSO4+H2
n Mg =6/24=0,25(mol)
n H2=n Mg =0,25(mol)
V H2=0,25.22,4=5,6(l)
b) 3H2+FE2O3-->2Fe+3H2O
n Fe2O3=32/160=0,2(mol)
->Fe2O3 dư
n Fe =2/3n H2=1/6(mol)
m Fe =1/6.56=28/3(g)
\(a,n_{Mg}=\dfrac{6}{24}=0,25\left(mol\right)\\ Mg+H_2SO_4\rightarrow MgSO_4+H_2\\ n_{H_2}=n_{Mg}=0,25\left(mol\right)\\ V_{H_2\left(\text{đ}ktc\right)}=0,25.22,4=5,6\left(l\right)\\ b,n_{Fe_2O_3}=\dfrac{32}{160}=0,2\left(mol\right)\\ 3H_2+Fe_2O_3\rightarrow\left(t^o\right)2Fe+3H_2O\\ n_{Fe}=2.n_{Fe_2O_3}=2.0,2=0,4\left(mol\right)\\ m_{Fe}=0,4.56=22,4\left(g\right)\)

\(19,6\rightarrow19,5\\ n_{Zn}=\dfrac{19,5}{65}=0,3\left(mol\right)\)
PTHH: Zn + 2HCl ---> ZnCl2 + H2
0,3----------------------->0,3
=> VH2 = 0,3.22,4 = 6,72 (l)
\(n_{Fe_2O_3}=\dfrac{19,2}{160}=0,12\left(mol\right)\)
PTHH: Fe2O3 + 3H2 --to--> 2Fe + 3H2O
LTL: \(0,12>\dfrac{0,3}{3}\) => Fe2O3 dư
\(n_{Fe}=\dfrac{2}{3}.0,3=0,2\left(mol\right)\\ \rightarrow m_{Fe}=0,2.56=11,2\left(g\right)\)
\(n_{Zn}=\dfrac{19,6}{65}=0,3\left(mol\right)\\
pthh:Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,3 0,6 0,3 0,3
\(V_{H_2}=0,3.22,4=6,72L\)
\(n_{Fe_2O_3}=\dfrac{19,2}{160}=0,12\left(mol\right)\\
pthh:Fe_2O_3+3H_2\rightarrow2Fe+3H_2O\)
\(ltl:\dfrac{0,12}{1}>\dfrac{0,3}{3}\)
= > Fe2O3 dư
\(n_{Fe}=n_{H_2}=0,3\left(mol\right)\\
m_{Fe}=0,3.56=16,8g\)

a, PT: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
Ta có: \(n_{Mg}=\dfrac{7,2}{24}=0,3\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Mg}=0,3\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,3.22,4=6,72\left(l\right)\)
b, PT: \(Fe_2O_3+3H_2O\underrightarrow{t^o}2Fe+3H_2O\)
Ta có: \(n_{Fe_2O_3}=\dfrac{19,2}{160}=0,12\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,12}{1}>\dfrac{0,3}{3}\), ta được Fe2O3 dư.
Theo PT: \(n_{Fe}=\dfrac{2}{3}n_{H_2}=0,2\left(mol\right)\)
\(\Rightarrow m_{Fe}=0,2.56=11,2\left(g\right)\)
Bạn tham khảo nhé!
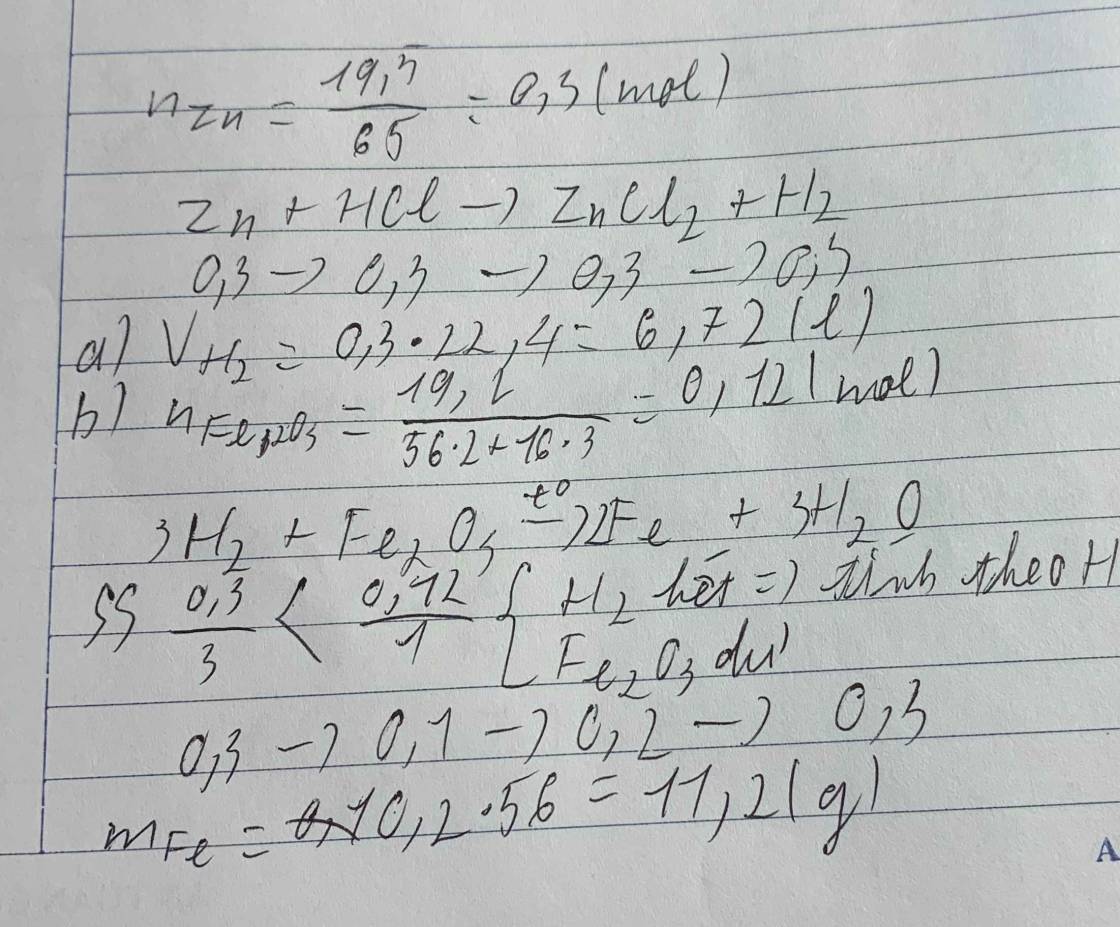
a)\(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\)
\(n_{Mg}=\dfrac{7,2}{24}=0,3mol\)
\(\rightarrow0,3molH_2\)\(\rightarrow V_{H2}=0,3.22,4=6,72l\)
b)\(H_2+Fe_2O_3\rightarrow3H_2O+2Fe\)
\(n_{Fe2O3}=\dfrac{19,2}{160}=0,12mol\)
\(\rightarrow0,24molFe\rightarrow m_{Fe}=0,24.56=13,44gam\)