Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu trả lời đúng là C.
PT: 2Al + 3H2SO4 → Al2(SO4)3 + 3H2
Từ phản ứng này ⇒ có thể điều chế khí H2
Khí H2 nhẹ hơn không khí nên úp ngược ống nghiệm sẽ thu được khí H2

a)6KMnO4--->3K2MnO4 + 3MnO2 + 3O2 (1)
2KClO3---> 2KCl + 3O2 (2)
Dựa vào phương trình trên ---> thu cùng lượng O2, KMnO4 cần nhiều số mol hơn, và khối lượng nhiều hơn.
b)6KClO3-->6KCl + 9O2 (3)
1,3--->Cùng số mol, KClO3 cho nhiều O2 hơn.
c)Giả sử cả 2 chất cùng có khối lượng là 100g
nKMnO4=50/79(mol)
nKClO3=40/49
Thay vào các phương trình phản ứng tính ra mO2
Cụ thể: KMnO4 cho ra 800/79 (g) O2
KClO3 cho ra 1920/49 (g) O2
---> Cùng m thì KClO3 cho nhiều g O2 hơn.
d) Giả sử cần điều chế 32 g O2
--->nO2=1 mol
--->nKMnO4=2 mol--->mKMnO4=316g
và nKClO3=2/3 mol--->nKClO3=245/3g
Ta có:
-1000g KMnO4 <=> 200000đ
316 g=========>63200đ
-1000g KClO3 <=> 300000đ
245/3g========> 24500đ
Vậy để điều chế cùng lượng O2, KClO3 có giá thành rẻ hơn.

nP = 3,1 : 31 = 0,1 (mol)
pthh : 4P + 5O2 -t--> 2P2O5 (1)
0,1--> 0,125 (mol)
=> VO2 = 0,125 .22,4 = 2,8(l)
pthh : 2KMnO4 -t--> K2MnO4 + MnO2 +O2 (2)
0,25<--------------------------- 0,125(mol)
=> mKMnO4 = 0,25 .158 = 39,5(g)
d ) (1) là Phản ứng hóa hợp
(2) là phản ứng phân hủy
nP = 3,1/31 = 0,1 (mol)
PTHH: 4P + 5O2 -> (t°) 2P2O5 (phản ứng hóa hợp)
Mol: 0,1 ---> 0,125
VO2 = 0,125 . 22,4 = 2,8 (l)
PTHH: 2KMnO4 -> (t°) K2MnO4 + MnO2 + O2 (phản ứng phân hủy)
nKMnO4 = 0,125 . 2 = 0,25 (mol)
mKMnO4 = 0,25 . 158 = 39,5 (g)

a)PTHH:2KClO\(_3\)➞\(^{t^o}\)2KCl+3O\(_2\)
b) n\(_{KClO_3}\)=\(\dfrac{m_{KClO_3}}{M_{KClO_3}}\)=\(\dfrac{12,15}{122,5}\)\(\approx\)0,1(m)
PTHH : 2KClO\(_3\) ➞\(^{t^o}\) 2KCl + 3O\(_2\)
tỉ lệ : 2 2 3
số mol : 0,1 0,1 0,15
V\(_{O_2}\)=n\(_{O_2}\).22,4=0,15.22,4=3,36(l)
c)PTHH : 2Zn + O\(_2\) -> 2ZnO
tỉ lệ : 2 1 2
số mol :0,3 0,15 0,3
m\(_{Zn}\)=n\(_{Zn}\).M\(_{Zn}\)=0,3.65=19,5(g)

PTHH: \(Cu_2S+2O_2\xrightarrow[]{t^o}2CuO+SO_2\)
a) Ta có: \(n_{Cu_2S}=\dfrac{100}{160}=0,625\left(mol\right)\) \(\Rightarrow n_{O_2\left(lýthuyết\right)}=1,25\left(mol\right)\)
\(\Rightarrow V_{O_2\left(thực\right)}=\dfrac{1,25\cdot22,4}{96\%}\approx29,17\left(l\right)\)
b) Sửa đề: "Tính khối lượng KMnO4 để hấp thụ hết SO2"
PTHH: \(5SO_2+2KMnO_4+2H_2O\rightarrow K_2SO_4+2MnSO_4+2H_2SO_4\)
Ta có: \(n_{SO_2\left(thực\right)}=n_{Cu_2S}\cdot96\%=0,6\left(mol\right)\)
\(\Rightarrow n_{KMnO_4}=0,24\left(mol\right)\) \(\Rightarrow m_{KMnO_4}=0,24\cdot158=37,92\left(g\right)\)
c) PTHH: \(SO_2+\dfrac{1}{2}O_2\xrightarrow[V_2O_5]{t^o}SO_3\)
Theo PTHH: \(n_{O_2}=\dfrac{1}{2}n_{SO_2}=0,3\left(mol\right)\) \(\Rightarrow V_{kk}=\dfrac{0,3\cdot22,4}{21\%}=32\left(l\right)\)
d) Bảo toàn nguyên tố Lưu huỳnh: \(n_{H_2SO_4\left(lýthuyết\right)}=n_{SO_2\left(thực\right)}=0,3\left(mol\right)\)
\(\Rightarrow n_{H_2SO_4\left(thực\right)}=0,3\cdot85\%=0,255\left(mol\right)\) \(\Rightarrow m_{ddH_2SO_4}=\dfrac{0,255\cdot98}{10\%}=249,9\left(g\right)\)


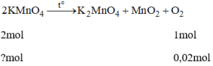
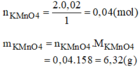

a)Các hình: 3,5,6,8
b) b/ Trong các hình đã chọn, hình dùng để điều chế oxi nhanh và có hiệu quả là: hình 6.
*Vì hình 6 khi đốt KClO3 có chất MnO2 làm chất xúc tác thì phản ứng sẽ xảy ra nhanh hơn và có hiệu quả.
Mình cảm ơn nhiều ạ ^^