
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


PTHH: 2Cu + O2 ---to→ 2CuO
Mol: x 0,5x
PTHH: 2Mg + O2 ---to→ 2MgO
Mol: 0,5x 0,25x (do số mol của Cu gấp đôi Mg)
Ta có: \(64x+24.0,25x=15,2\Leftrightarrow x=\dfrac{38}{175}\left(mol\right)\)
\(\Rightarrow n_{O_2}=0,5.\dfrac{38}{175}+0,25.\dfrac{38}{175}=\dfrac{57}{350}\left(mol\right)\)
\(\Rightarrow V_{O_2}=\dfrac{57}{350}.22,4=3,648\left(l\right)\)
\(\Rightarrow V_{kk}=3,648.5=18,24\left(l\right)\)

a)
ta có \(n_{N_2}=\dfrac{4,2}{28}=0,15\left(mol\right)\)
\(\Rightarrow V_{N_2}=0,15.22,4=3,36l\)
ta có \(n_{O_2}=\dfrac{3,2}{32}=0,1\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,1.22,4=2,24l\)
b)
ta có \(n_{SO_2}=\dfrac{32}{64}=0,5\left(mol\right)\)
\(\Rightarrow V_{SO_2}=0,5.22,4=11,2l\)
ta có \(n_{O_2}=\dfrac{32}{32}=1\left(mol\right)\)
\(\Rightarrow V_{O2}=1.22,4=22,4l\)
c)
ta có \(n_{H_2}=\dfrac{2}{2}=1\left(mol\right)\)
\(\Rightarrow V_{H_2}=1.22,4=22,4l\)
ta có \(n_{O_2}=\dfrac{8}{32}=0,25\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,25.22,4=5,6l\)
d)
ta có \(n_{N_2}=\dfrac{8,4}{28}=0,3\left(mol\right)\)
\(\Rightarrow V_{N_2}=0,3.22,4=6,72l\)
ta có \(n_{O_2}=\dfrac{6,4}{32}=0,2\left(mol\right)\)
\(\Rightarrow V_{N_2}=0,2.22,4=4,48l\)

a/ Ta có
- \(Cl=35,5đvC\)
- Đơn chất \(Cl=71đvC\)
- Số nguyên tử Cl trong 1 phân tử Cl \(=\dfrac{71}{35,5}=2\)
Vậy: Số nguyên tử Cl trong 1 phân tử Cl là 2


Bài 1:
1) Đặt CTHH của oxit sắt là \(Fe_xO_y\)
Ta có: \(\dfrac{m_{Fe}}{m_O}=\dfrac{7}{3}\)
\(\Rightarrow\dfrac{56x}{16y}=\dfrac{7}{3}\Leftrightarrow\dfrac{x}{y}=\dfrac{7}{3}.\dfrac{16}{56}=\dfrac{2}{3}\)
Vậy CTHH của oxit sắt là Fe2O3
2) \(n_{HCl}=\dfrac{35,04}{36,5}=0,96\left(mol\right)\)
Đặt CTHH của oxit sắt là \(Fe_xO_y\)
PTHH: \(Fe_xO_y+2yHCl\rightarrow FeCl_{2y/x}+yH_2O\)
\(\dfrac{0,48}{y}\)<----0,96
\(\Rightarrow M_{Fe_xO_y}=\dfrac{27,84}{\dfrac{0,48}{y}}=58y\left(g/mol\right)\)
`=> 56x + 16y = 58y`
\(\Leftrightarrow\dfrac{x}{y}=\dfrac{3}{4}\)
Vậy CTHH của oxit sắt là Fe3O4
Câu 2:
Ta có: \(\left\{{}\begin{matrix}p+e+n=40\\n-p=1\\p=e\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p=e=13\\n=14\end{matrix}\right.\)
Vậy nguyên tố X là nhôm (Al)
Câu 3:
Bạn tham khảo ở đây nhé mình lười không muốn gõ lại acc này đúng tên và cau trả lời của mình rồi: https://olm.vn/cau-hoi/nung-m-gam-hon-hop-a-gom-kmno4-va-kclo3-thu-duoc-chat-ran-b-va-khi-oxi-luc-do-kclo3-bi-phan-huy-hoan-toan-con-kmno4-bi-phan-huy-khong-hoan-toan-tron.6301688835253
Câu 4: Sửa đề 16,75% -> 16,47%
\(n_{O_2}=\dfrac{1,68}{22,4}=0,075\left(mol\right)\)
Áp dụng ĐLBTKL:
\(m_B=m_A-m_{O_2}=15,15-0,075.32=12,75\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_N=\dfrac{12,75.16,47\%}{14}=0,15\left(mol\right)\\n_O=\dfrac{12,75.37,65\%}{16}=0,3\left(mol\right)\\n_K=\dfrac{12,75-0,15.14-0,3.16}{39}=0,15\left(mol\right)\end{matrix}\right.\)
Đặt CTHH của B là \(K_xN_yO_z\)
\(\Rightarrow x:y:z=0,15:0,15:0,3=1:1:2\)
Vậy B là KNO2
BTNT O: \(n_{O\left(A\right)}=0,075.2+0,3=0,45\left(mol\right)\)
Đặt CTHH của A là \(K_aN_bO_c\)
\(\Rightarrow a:b:c=0,15:0,15:0,45=1:1:3\)
Vậy A là KNO3

Câu 9 :
a) $FeO + H_2SO_4 \to FeSO_4 + H_2O$
$n_{FeSO_4} =n_{H_2SO_4} = n_{FeO} = \dfrac{7,2}{72} = 0,1(mol)$
$m_{dd\ H_2SO_4} = \dfrac{0,1.98}{24,5\%} = 40(gam)$
$m_{dd\ sau\ pư} = 40 + 7,2 = 47,2(gam)$
Gọi $n_{FeSO_4.7H_2O} = a(mol)$
Sau khi tách :
$m_{dd} = 47,2 - 278a(gam)$
$n_{FeSO_4} = 0,1 - a(mol)$
Suy ra :
$C\% = \dfrac{152(0,1 - a)}{47,2 - 278a}.100\% = 12,18\%$
$\Rightarrow a = 0,08$
$m = 0,08.278 =22,24(gam)$


Bài 6 :
\(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
Pt : \(Fe+2HCl\rightarrow FeCl_2+H_2|\)
1 2 1 1
0,1 0,1 0,1
a) \(n_{H2}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,1.22,4=2,24\left(l\right)\)
b) \(n_{FeCl2}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
⇒ \(m_{FeCl2}=0,1.127=12,7\left(g\right)\)
Chúc bạn học tốt




 giúp em với ạ cần gấp á :(((
giúp em với ạ cần gấp á :((( giúp em câu 8 câu 9 với em cần gấp ạ
giúp em câu 8 câu 9 với em cần gấp ạ
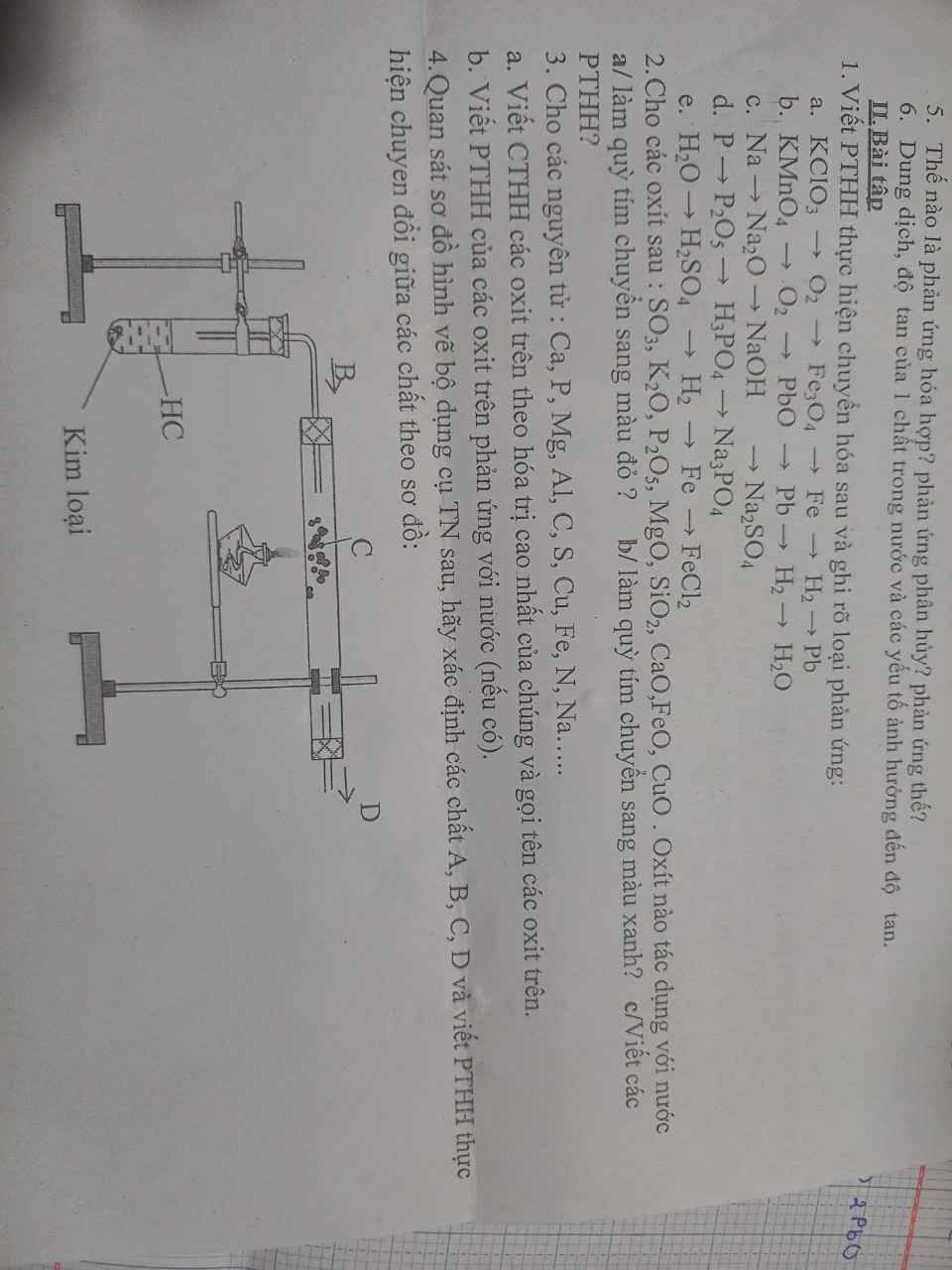 mn giải giúp em với ạ em đag cần gấp , em cảm ơn
mn giải giúp em với ạ em đag cần gấp , em cảm ơn



CaO+H2O->Ca(OH)2 canxi hidroxit (hóa hợp)
2K+2H2O->2KOH+H2 kali hidroxit (thế)
SO3+H2O->H2SO4 axit sunfuric (hóa hợp)