
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



Câu 4 :
a. \(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
PTHH : Zn + 2HCl -> ZnCl2 + H2
0,2 0,4 0,2 0,2
b. \(V_{H_2}=0,2.22,4=4,48\left(l\right)\)
c. \(m_{HCl}=0,4.36,5=14,6\left(g\right)\)
\(\Rightarrow m_{ddHCl10\%}=\dfrac{14,6.100}{10}=146\left(g\right)\)
10% là nồng độ của dung dịch axit clohidric tức là cho biết số gam chất tan trong 100g dd đó.
a. \(PTHH:Zn+2HCl\rightarrow ZnCl_2+H_2\)
b. \(n_{Zn}=\dfrac{m_{Zn}}{M_{Zn}}=\dfrac{13}{65}=0,2\left(mol\right)\)
\(PTHH:Zn+2HCl\rightarrow ZnCl_2+H_2\)
Mol : 1 : 2 : 1 : 1
Mol : 0,2 → 0,4 → 0,2 → 0,2
\(\Rightarrow n_{H_2}=0,2\left(mol\right)\)
\(\Rightarrow V_{H_2}=n_{H_2}.22,4=0,2.22,4=4,48\left(l\right)\)
c. \(n_{Zn}=\dfrac{m_{Zn}}{M_{Zn}}=\dfrac{13}{65}=0,2\left(mol\right)\)
\(PTHH:Zn+2HCl\rightarrow ZnCl_2+H_2\)
Mol : 1 : 2 : 1 : 1
Mol : 0,2 → 0,4 → 0,2 → 0,2
\(\Rightarrow n_{HCl}=0,4\left(mol\right)\)
\(\Rightarrow m_{HCl}=n_{HCl}.M_{HCl}=0,4.36,5=14,6\left(g\right)\)

Đặt nAl = nFe = x
=> 27x + 56x = 83
=> x = 0,1
\(n_{AgNO_3}=0,1.2=0,2\left(mol\right);n_{Cu\left(NO_3\right)_2}=0,1.1,5=0,15\left(mol\right)\)
=> \(n_{NO_3^-}=0,2.1+0,15.2=0,5\left(mol\right)\)
Dung dịch sau phản ứng : Al3+ , Fe2+, NO3-
Bảo toàn điện tích, ta có : \(n_{Al}.3+n_{Fe}.2=n_{NO^-_3}.1\)
=> Sau phản ứng Al, Fe hết, Ag+, Cu2+ bị khử hết
=>Kim loại được giải phóng : Ag, Cu
Bảo toàn nguyên tố Ag : nAg = nAgNO3 = 0,2(mol)
=> m Ag = 108.0,2 =21,6 (g)
Bảo toàn nguyên tố Cu : nCu = nCu(NO3)2 = 0,15(mol)
=> m Cu = 64.0,15 =9,6 (g)





Cho 130g kim loại kẽm tác dụng với axit clohidric thu được 272g kẽm clorua và 4g khí Hidro.
a)Lập phương trình hóa học?
b)Viết biểu thức liên hệ về khối lượng giữa các chất phản ứng?
c)Tính khối lượng axit clohidric đã tham gia phản ứng?

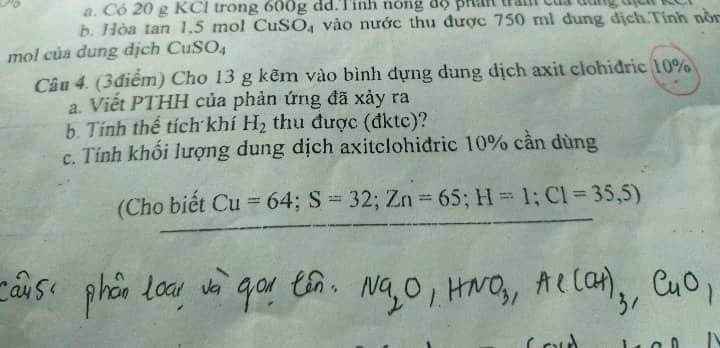





 Mn giúp e bài này vs ạ , e cảm ơn nhìu ạ!
Mn giúp e bài này vs ạ , e cảm ơn nhìu ạ!
pH=13 -----> pOH= 1 => [OH-]= 0,1M
=> \(n_{OH^-}=0,1.1,2=0,12\left(mol\right)\)
\(n_{CO_2}=\dfrac{1,68}{22,4}=0,075\left(mol\right)\)
Lập tỉ lệ : \(\dfrac{n_{OH^-}}{n_{CO_2}}=\dfrac{0,12}{0,075}=1,6\)
=> Tạo 2 muối CO32- (x_mol) và HCO3- (y_mol)
Ta có hệ : \(\left\{{}\begin{matrix}x+y=0,075\\2x+y=0,12\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}x=0,045\\y=0,03\end{matrix}\right.\)
*Nếu làm bài tập trắc nghiệm có thể áp dụng CT nhanh sau để tính số mol muối CO32- và HCO3-
\(n_{CO_3^{2-}}=n_{OH^-}-n_{CO_2}=0,12-0,075=0,045\)
Bảo toàn nguyên tố C => \(n_{HCO_3^-}=n_{CO_2}-n_{CO_3^{2-}}=0,075-0,045=0,03\left(mol\right)\)
Phản ứng OH- với CO2 ưu tiên tạo kết tủa trước
\(n_{BaCO_3}=\dfrac{7,88}{197}=0,04\left(mol\right)\)
Vì \(n_{BaCO_3}< n_{CO_3^{2-}}\) ( 0,04< 0,045)
=> CO32- còn dư
=> Dung dịch gồm : CO32- dư ( 0,045- 0,04 = 0,005_mol ) , HCO3- =0,03(mol) , Na+ và K+
=> \(m_{\left(Na^+,K^+\right)}=3,53-m_{CO_3^{2-}}-n_{HCO_3^-}=3,53-0,005.60-0,03.61=1,4\)(g)
\(n_{OH^-}=2n_{H_2}+2n_{O\left(trongoxit\right)}=0,12\) (mol)
\(\Rightarrow n_O=\dfrac{0,12-0,005.2}{2}=0,055\left(mol\right)\)
=>mX= 1,4 + 0,04.137 + 0,055.16= 7,76 (g)
=> Chọn C