Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

PTHH:
\(CO_2+Ca\left(OH\right)_2\rightarrow CACO_3+H_2O\)
Khí còn lại bay ra là khí \(CH_4\rightarrow CH_4\)được làm sạch
=> Chọn A. Dung dịch Ca(OH)\(_2\)

Ta có: mC2H4 = m bình tăng = 2,8 (g)
\(\left\{{}\begin{matrix}\%m_{C_2H_4}=\dfrac{2,8}{4}.100\%=70\%\\\%m_{CH_4}=30\%\text{ }\end{matrix}\right.\)
Bạn tham khảo nhé!

nBr2 = 0,125 mol
Khi đốt cháy nA = 0,25 mol
mNaOH ban đầu = 36g => nNaOH = 0,9 mol
Gọi x, y lần lượt là số mol của CO2 và H2O
mdd = 180 + 44x + 18y
Vì NaOH dư do đó chỉ tạo muối trung hòa
CO2 +2NaOH → Na2CO3 + H2O
x 2x
nNaOH dư = 0,9 – 2x
có 2 , 75 % = 40 ( 0 , 9 - 2 x ) 180 + 44 x + 18 y . 100 % (1)
=> 81,21x + 0,495y = 31,05n
2,8 lít khí A tác dụng với 0,125 mol Br2
=> 5,6 lít khí A tác dụng với 0,25 mol Br2
Gọi số mol khí của CH4, C2H4 và C2H2 lần lượt là a; b; c
Ta có a + b + c = 0,25 mol
Và b + 2c = 0,25
=> a = c
=> khi đốt cháy hỗn hợp A cho nCO2 = nH2O
Thay vào (1) => x = y = 0,38 mol
Bảo toàn C, H khi đốt cháy ta có
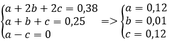
=> %VCH4 = %VC2H2 = 48%
%VC2H4 = 4%

a/ Xác định kim loại M
nH2SO4 ban đầu = 78,4.6,25:100=0.05 mol
Goi số mol MO là a mol, mMO = (M+16).a
MO+H2SO4---MSO4+H2O(1)
a mol amol amol
Số mol axit dư sau phản ứng (1): 0,05-a mol
mdd sau phản ứng: (m+16)a+78,4
Theo bài ra ta có: 2,433=100.(0,05-a).98/[(m+16)a+78,4] (I)
Mặt khác: MO+CO---M+CO2 (2)
a mol a mol a mol amol
Theo bài ra CO2 tham gia phản ứng hết, các phản ứng có thể xảy ra:
CO2+2NaOH--->Na2CO3+H2O
b 2b b b
CO2+NaOH--->NaHCO3
c c c
Khối lượng muối tạo thành: 100b+84c=2,96
- Nếu NaOH dư không xảy ra phản ứng (3). Tức là c = 0 mol,
b = a = 2,96 : 106 = 0,028 mol. Thay a = 0,028 vào (I) ta tìm được M = 348,8 (loại).
- Nếu NaOH phản ứng hết: 2b + c = 0,5 . 0,1 = 0,05 (III)
Từ (II) và (III) ta có : 106 b + 84(0,05 – 2b) = 2,96
62b = 1,24 suy ra: b= 0,02 và c = 0,01
Theo 2, 3 và 4, n co2 = 0,03= n MO = a = 0,03.
Thay giá trị a = 0,03 và (I) ta có: 0,07299M = 4,085
M = 56 vậy kim loại M là Fe, mMO=(56+16).0,03= 2,16 g
b/ Dung dịch E gồm FeSO4 0,03 mol và H2SO4 dư 0,02 mol. Khi cho Al phản ứng hoàn toàn tạo 1,12 gam chất rắn, H2SO4 phản ứng hết.
2Al+3H2SO4---->Al2(SO4)3+3H2
2Al+3FeSO4----->Al2(SO4)3+3Fe
Khối lượng Fe trong dung dịch E : 56 . 0,03 = 1,68 gam > 1,12 gam
Như vậy FeSO4 còn dư thì Al tan hết. Vây t = 1,12: 56 =0,02 mol
Vây n Al = 0,04 : 3 + 0,04:3 = (0,08 : 3) mol
Vây khối lượng x = 0,08: 3 . 27 = 0,72 gam

Gọi số mol của C2H4 và C2H2 lần lượt là x và y
Ta có nBr2 phản ứng = nC2H4 +2nC2H2 = x + 2y = 0,07
MX= 26,5
=> 28x+26y = 26,5 (x+y)
Giải hệ được x = 0,01 và y = 0,03
=> %C2H4 = 25% và %C2H2 = 75%

n Br2=\(\dfrac{32}{160}\)=0,2 mol
C2H2+2Br2->C2H2Br4
0,1------0,2 mol
=>%VC2H2=\(\dfrac{0,1.22,4}{5,6}\).100=40%
=>%VCH4=100-40=60%
=>n CH4=\(\dfrac{5,6-0,1.22,4}{22,4}\)=0,15 mol
CH4+2O2-to>CO2+2H2O
0,15----0,3
C2H2+\(\dfrac{5}{2}\)O2-to>2CO2+H2O
0,1-----0,25 mol
=>VO2=(0,3+0,25).22,4=12,32l

Nếu bạn đổi bình thì sau khi tác dụng với đ hcl tạo ra khí cl2 chắc bạn hiểu rồi. Nhưng bạn nên biết khí cl2 sau pưg sẽ lẫn 2 thứ là khí HCl(axit có thể ở dạng lỏng hoặc khí bạn nên tìm hiểu về nó) và nước Nếu bạn đổi lôn bình 2 với bình 1 sẽ xảy ra puwg
HCl + H2SO4 ---) H2O + SO2 + Cl2
nó sẽ lẫn thêm khí So2
Để tránh lằng nhằng thì bình 1 họ cho khí clo qua dd NaCl vì dd này sẽ giữ khí Hcl rất tốt. Vậy là loại đc khí axit
Sau đó sục nó qua dd H2SO4 đặc vì nó có tính háo nước(hút nước tốt)
NaOH + Cl2 --) NaCl + NaClO + H2O
do khí cl2 rất độc nên ko cho nó thoát ra ngoài mà lượng phản ứng không hề đáng kể hay có thể nói là giữ ko cho khí đi qua
Đáp án C