Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
Lấy BaCl2 cho lần lượt vào 3 mẫu thử.
Các phương trình phản ứng xảy ra:
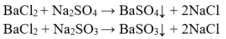
Mẫu không có kết tủa là HCl. Lấy HCl cho vào kết tủa, BaSO3 tan.
![]()

Trích mẫu thử
Cho dung dịch $Ba(HCO_3)_2$ vào
- mẫu thử tạo kết tủa trắng là $Na_2CO_3$
$Ba(HCO_3)_2 + Na_2CO_3 \to BaCO_3 + 2NaHCO_3$
- mẫu thử tạo khí không màu là HCl
$Ba(HCO_3)_2 + 2HCl \to BaCl_2 + 2CO_2 + 2H_2O$
- mẫu thử vừa tạo khí và kết tủa là $H_2SO_4$
$Ba(HCO_3)_2 + H_2SO_4 \to BaSO_4 + 2CO_2 + 2H_2O$
Cho $H_2SO_4$ vừa nhận được vào hai chất còn :
- chất nào tạo kết tủa là $BaCl_2$
$BaCl_2 + H_2SO_4 \to BaSO_4 + 2HCl$
- chất nào không ht là NaCl
*Cách khác
- Dùng quỳ tím
+) Hóa xanh: Na2CO3
+) Hóa đỏ: HCl và H2SO4 (Nhóm 1)
+) Không đổi màu: NaCl và BaCl2 (Nhóm 2)
- Đổ dd Na2CO3 đã biết vào nhóm 2
+) Xuát hiện kết tủa: BaCl2
PTHH: \(Na_2CO_3+BaCl_2\rightarrow2NaCl+BaCO_3\downarrow\)
+) Không hiện tượng: NaCl
- Đổ dd BaCl2 đã biết vào nhóm 1
+) Xuất hiện kết tủa: H2SO4
PTHH: \(BaCl_2+H_2SO_4\rightarrow2HCl+BaSO_4\downarrow\)
+) Không hiện tượng: HCl

Đáp án A
Để phân biệt các dung dịch: H C l , K O H , C a ( N O 3 ) 2 , B a C l 2 người ta dùng quì tím và A g N O 3 vì:
|
|
HCl |
KOH |
C a ( N O 3 ) 2 |
B a C l 2 |
| Quì tím |
Đỏ |
Xanh |
Tím |
Tím |
| A g N O 3 |
x |
x |
Không hiện tượng |
Kết tủa trắng |
Dấu x là đã nhận biết được rồi
Phương trình hóa học: B a C l 2 + 2 A g N O 3 → 2 A g C l ↓ + B a ( N O 3 ) 2

Đáp án A
Trích mẫu thử
Cho quỳ tím vào các mẫu thử
- mẫu thử làm quỳ tím hóa đỏ là HCl,H2SO4. Gọi là nhóm 1
- mẫu thử làm quỳ tím hóa xanh là NaOH
Cho nhóm 1 vào các mẫu thử còn lại :
- mẫu thử nào tạo kết tủa trắng là H2SO4
\(BaCl_2 + H_2SO_4 \to BaSO_4 + 2HCl\)
- mẫu thử không hiện tượng là HCl
Cho dung dịch H2SO4 vừa nhận được vào mẫu thử còn :
- mẫu thử tạo kết tủa trắng là BaCl2
Cho dung dịch BaCl2 vào mẫu thử còn :
- mẫu thử tạo kết tủa trắng là Na2SO4
\(BaCl_2 + Na_2SO_4 \to BaSO_4 + 2NaCl\)
- mẫu thử không hiện tượng là NaCl

Trích mẫu thử rồi cho AgNO3 vào lần lượt các dung dịch
- Nhóm 1: có kết tủa trắng xuất hiện là: NaCl, BaCl2.
- Nhóm 2: không có hiện tượng là: NaNO3, Ba(NO3)2.
Ở mỗi nhóm dùng Na2SO4 để phân biệt
- Có kết tủa trắng xuất hiện là: BaCl2.
- Có kết tủa trắng xuất hiện là: Ba(NO3)2

Đáp án B
Lời giải
Dùng dung dịch BaCl2 để phân biệt các dung dịch : H2SO4 loãng, Ba(OH)2 và HCl
|
|
H2SO4 loãng |
Ba(OH)2 |
KCl |
| Dung dịch BaCl2 |
Kết tủa trắng |
Không hiện tượng |
Không hiện tượng |
| Dung dịch H2SO4 |
|
Kết tủa trắng |
Không hiện tượng |
Đầu tiên dùng dung dịch BaCl2 sẽ nhận biết được H2SO4 loãng:
![]()
Dùng dung dịch H2SO4 vừa nhận biết được để nhận biết các dung dịch Ba(OH)2 và HCl:
![]()

Chọn thuốc thử Ba(OH)2
Lấy mỗi dung dịch axit một ít cho vào ống nghiệm.
- Cho từng giọt dung dịch Ba(OH)2 và các ống nghiệm chứa các axit đó:
Có kết tủa trắng là ống đựng H2SO3 và H2SO4, đó là kết tủa BaSO3 và BaSO4
⇒ Nhận biết được ống chứa HCl (không có hiện tượng gì)
- Lấy dung dịch HCl vừa nhận biết được cho vào các kết tủa:
Kết tủa tan được và có khí bay ra BaSO3, suy ngược lên ta thấy dung dịch trong ống nghiệm ban đầu là H2SO3
Kết tủa không tan trong axit là BaSO4, suy ngược lên ta thấy dung dịch trong ống nghiệm ban đầu là H2SO4.
Ba(OH)2 + H2SO3 → BaSO3 ↓ + 2H2O
Ba(OH)2 + H2SO4 → BaSO4 ↓ + 2H2O
BaSO3 + 2HCl → BaCl2 + SO2 ↑ + H2O

1. Cho HNO3 tác dụng với từng chất:
- Có tác dụng -> Na2CO3
- Không tác dụng -> AgNO3, KNO3
Cho từng chất tác dụng với Na2CO3 vừa nhận biết được:
- Có tác dụng -> AgNO3
- Không tác dụng -> KNO3
2. Cho H2SO4 tác dụng với từng chất:
- Có tác dụng:
+ Kết tủa trắng -> BaCl2
+ Có khí không màu, mùi hắc thoát ra -> K2SO3
- Không tác dụng -> NaCl
3. Cho thử quỳ tím:
- Đổi màu xanh -> Ba(OH)2
- Đổi màu đỏ -> HCl, H2SO4 (1)
- Không đổi màu -> NaCl, K2SO3 (2)
Cho từng chất (1) tác dụng với từng chất (2), có 2 cặp chất tác dụng với nhau:
- HCl và K2SO4
- NaCl và H2SO4

Cho quỳ tím lần lượt vào từng dung dịch :
- Hóa đỏ : H2SO4 , HCl (1)
- Không HT : BaCl2
Cho dung dịch BaCl2 lần lượt vào các chất ở (1) :
- Kết tủa trắng : H2SO4
- Không HT : HCl
BaCl2 + H2SO4 => BaSO4 + 2HCl