Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án B
2Al + 6HCl → 2AlCl3 + 3H2↑. Bảo toàn khối lượng:
mAl + mdung dịch HCl = mdung dịch sau phản ứng + mH2.
⇒ mtăng = mdung dịch sau – mdung dịch HCl = mAl – mH2 = 14,4(g).
Mặt khác, nH2 = 1,5.nAl ||⇒ giải hệ có: nAl = 0,6 mol; nH2 = 0,9 mol.
► mmuối = 0,6 × 133,5 = 80,1(g) ⇒ chọn B.

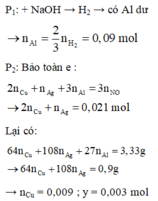
Trong 6,66g B có : 0,018 mol Cu ; 0,006 mol Ag ; 0,18 mol Al
Dung dịch C + HCl không tạo kết tủa → không có Ag+
+) Dung dịch D + thanh Fe
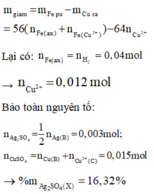
Đáp án A

Đáp án B
Do dung dịch Y tăng 21,28 gam.
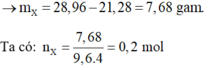
Do vậy ta giải được số mol CO2 và NO trong X lần lượt là 0,06 mol và 0,08 mol.
Vậy số mol FeCO3 là 0,06 mol.
Do khi thêm AgNO3 vào Y có xuất hiện NO nên H+ dư nên Y không có NO3- dư.
Bảo toàn N:
![]()
Gọi a,b lần lượt là số mol Mg, Fe3O4, c là số mol HCl.
Do vậy kết tủa chứa AgCl c mol và Ag.
![]()
Do cho AgNO3 vào sinh ra 0,03 mol NO nên H+ dư 0,12 mol.
Bảo toàn e kết hợp bảo toàn điện tích:
c = 0,04 + 8b + 0,06.2 + 0,08.3 + 0,06.8 + 0,04.8 + 0,12
Bảo toàn e:
![]()
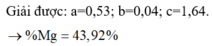

Số mol H2 là nH2 = 0,6/2 = 0,3(mol)
PTHH : Mg + 2HCl → MgCl2 + H2 ↑ (1)
Zn + 2HCl → ZnCl2 + H2 ↑ (2)
Gọi x, y lần lượt là số mol của Mg và Zn trong dung dịch x, y > 0
nH2 = x + y = 0,3 mol.
mhh = 24x + 65y = 15,4.
Khối lượng muối là m = x(24 + 71) + y(65 + 71)
m = 24x + 65y + 71(x + y) = 15,4 + 71.0,3 = 36,7 (g)

Mg + 2HCl →→ MgCl2 + H2 (1)
Al + 3HCl →→ AlCl3 + 3232H2 (2)
Đặt nMg=a
nAl=b
Ta có
24a+27b=7.8 g (3)
⇒⇒ 0,8g mất đi là do H2 bay hơi ⇒nH2=0,82=0,4(mol)⇒nH2=0,82=0,4(mol)
⇒⇒ a+3/2b=0.4 (4)
Giải hệ 3 và 4 ta có:
a=0,1;b=0,2
Theo PTHH 1 và 2 ta có;
nHCl(1)=2nMg=0,2(mol)
nHCl(2)=3nAl=0,6(mol)
∑nHCl=0,2+0,6=0,8(mol)

Đơn giản : áp dụng bảo toàn ng tố và bt điện tích là ok.
Ta tính đk tổng mol H+(hcl,h2so4)=0,2\(+0,1\times2=0,4mol\) Mà mol H2:0,195mol →mol H+p/ư=0,195\(\times2=0,39mol\)
TH1 : hcl hết ,H2SO4 dư .→mol H2SO4(pư)=\(\frac{0,39-0,2}{2}=0,095mol\) Suy ra : mol (cl-)=0,2 và mol (so42-)=0,095mol
Suy ra m(muối)=mAl+mMg+m(so42-)+m(cl-)=3,87+\(0,095\times96+0,2\times35,5=20,09g\)
TH2 :H2So4 hết ,HCL dư →mol HCl(pư)=0,39-,\(0,1\times2=0,19mol\) ,mol (SO42-)=0,1mol
Tương tự tính m(muối)=20,215g ,,,,,,,,,,,,,Mình giải 2 TH tháy đáp án nào có thì khoanh lun he
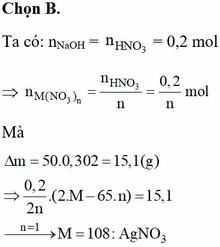


Giải thích: Đáp án B
2Al + 6HCl → 2AlCl3 + 3H2
Hướng dẫn giải :
mdd tắng= m – mH2 = 27nAl – 3nAl → nAl=0,6 mol → mAlCl3 =0,6.133,5=80,1 g
dễ thế , đi copy trang khác xong vô paste lại là xong bạn nhỉ?