Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Bài 1:
\(n_{KNO_3}=\dfrac{20}{101}=0,198\left(mol\right)\)
\(C_M=\dfrac{n}{V}=\dfrac{0,198}{0,85}=0,233M\)
Bài 2:
\(C_M=\dfrac{n}{V}=\dfrac{0,5}{0,75}=0,66M\)
Bài 3:
\(n_{KNO_3}=2.0,5=1\left(mol\right)\)
\(m_{KNO_3}=1.101=101\left(g\right)\)
Bài 4:
\(C\%=\dfrac{20}{600}.100=3,33\%\)
Bài 1:
\(n_{KNO_3}=\dfrac{20}{101}=0,198\left(mol\right)\)
\(C_{M_{ddKNO_3}}=\dfrac{0,198}{0,85}\approx0,23M\)
Bài 2:
\(C_{M_{ddKCl}}=\dfrac{0,5}{0,75}\approx0,667M\)
Bài 3:
\(n_{KNO_3}=0,5.2=1\left(mol\right)\Rightarrow m_{KNO_3}=1.101=101\left(g\right)\)
Bài 4:
\(C\%_{ddKCl}=\dfrac{20.100\%}{600}=3,333\%\)

a) CM MgCl2 = 0,5/1,5 = 0,33M
b) n CuSO4 = 400/160 = 2,5(mol)
CM CuSO4 = 2,5/4 = 0,625M
a) `CM_(MgCl_2) = (0,5)/(1,5)`\(\approx\)`0,33 M`
b) `n_(CuSO_4)=2,5(mol)`
→ `CM_(CuSO_4)=(2,5)/4=0,625 M`

\(1,C_{M\left(HCl\right)}=\dfrac{0,75}{0,5}=1,5M\\ 2,n_{Ca\left(OH\right)_2}=\dfrac{37}{74}=0,5\left(mol\right)\\ C_{M\left(Ca\left(OH\right)_2\right)}=\dfrac{0,5}{1,5}=0,33M\\ 3,n_{NaOH}=0,25+\dfrac{20}{40}=0,75\left(mol\right)\\ C_{M\left(NaOH\right)}=\dfrac{0,75}{2}=0,375M\\ 4,n_{H_2SO_4}=\dfrac{49}{98}=0,5\left(mol\right)\\ C_{M\left(H_2SO_4\right)}=\dfrac{0,5}{2}=0,25M\)

`1) C_[M_[HCl]] = [ 0,75 ] / [ 0,5 ] = 1,5 (M)`
_____________________________________________
`2)n_[Ca(OH)_2] = 37 / 74 = 0,5 (mol)`
`-> C_[M_[Ca(OH)_2]] = [ 0,5 ] / [ 1,5 ] ~~ 0,33 (M)`
_____________________________________________
`3) n_[NaOH] = 0,25 + 20 / 40 = 0,75 (mol)`
`-> C_[M_[NaOH]] = [ 0,75 ] / 2 = 0,375 (M)`
_____________________________________________
`4) n_[H_2 SO_4] = 49 / 98 = 0,5 (mol)`
`-> C_[M_[H_2 SO_4]] = [ 0,5 ] / 2 = 0,25 (M)`
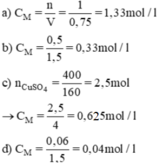
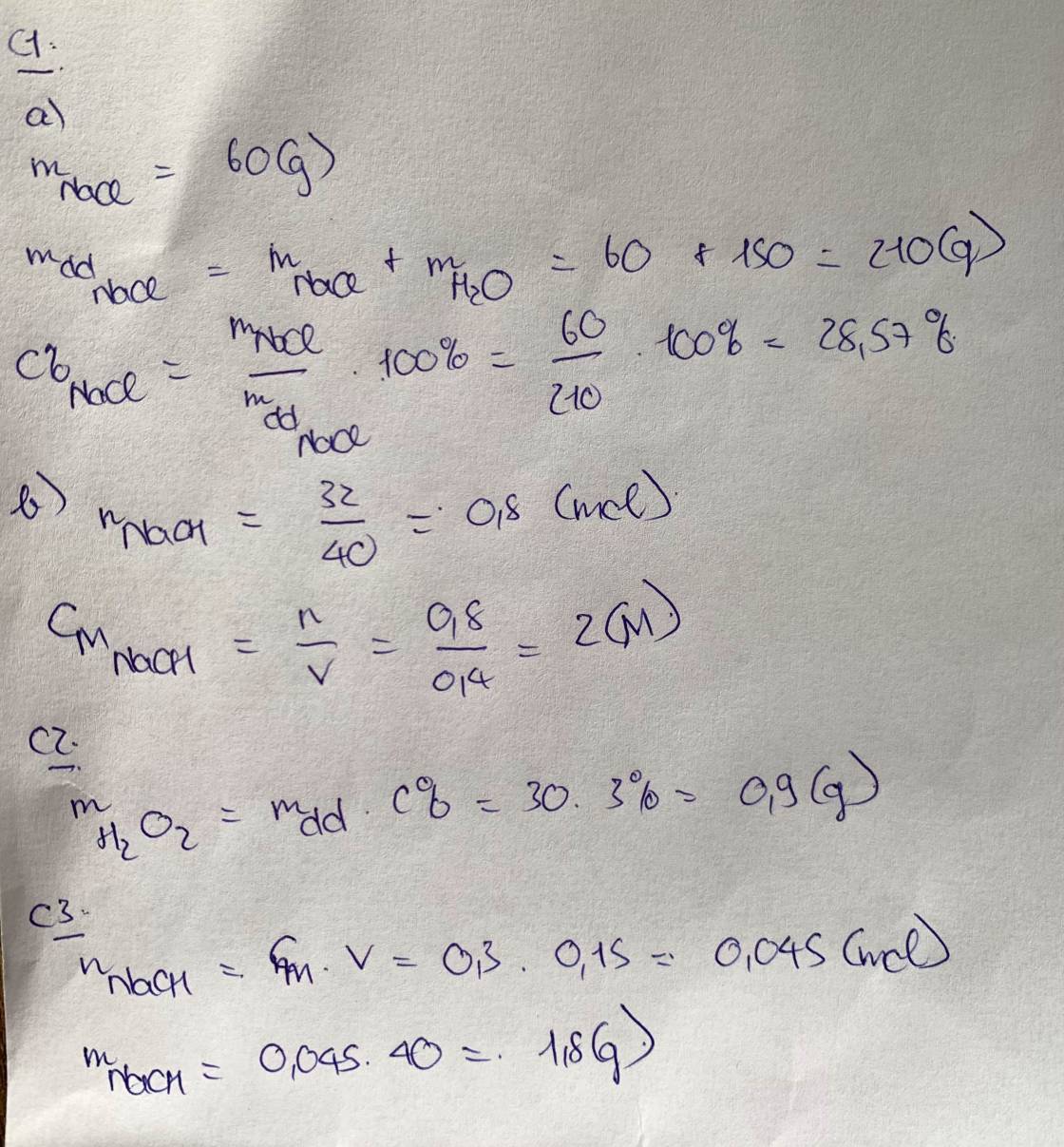
Câu 1:
a) \(C\%=\dfrac{15}{15+45}.100\%=25\%\)
b) \(C_M=\dfrac{0,5}{1,5}=0,33M\)
Câu 2:
a) \(n_{NaOH}=0,5.1=0,5\left(mol\right)=>m_{NaOH}=0,5.40=20\left(g\right)\)
b) \(n_{HCl}=0,2.0,5=0,1\left(mol\right)=>m_{HCl}=0,1.36,5=3,65\left(g\right)\)