Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn D
Ở ống (4) vừa tăng diện tích tiếp xúc của chất phản ứng vừa tăng nhiệt độ phản ứng → khí thoát ra nhanh nhất.

- Ta có phương trình: HCl + CaCO3 → CaCl2 + CO2↑ + H2O
=> Khi cho mẩu đá vôi tác dụng với dung dịch HCl thì có khí không màu thoát ra, khí đó là carbon dioxide
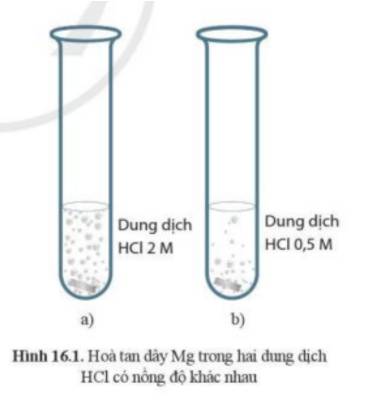
- Nồng độ HCl càng cao thì tốc độ phản ứng diễn ra càng nhanh.
- Giải thích: để phản ứng xảy ra, cần phải có sự va chạm giữa HCl và CaCO3. Ở ống nghiệm 2, nồng độ HCl lớn gấp đôi ở ống nghiệm 1, do vậy số va chạm của HCl và CaCO3 (trong cùng 1 đơn vị thời gian) sẽ lớn hơn, từ đó tốc độ phản ứng ở ống nghiệm 2 là lớn hơn

- Ở ống nghiệm (a) có hiện tượng sủi bọt khí nhiều hơn
=> Phản ứng ở ống nghiệm (a) xảy ra mãnh liệt hơn
=> Dây Mg ở ống nghiệm (a) sẽ bị tan hết trước
Mg + 2HCl → MgCl2 + H2↑

ống (1): hạt kẽm tan dần và có khí thoát ra
\(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
ống (2): ko có hiện tượng gì do Hcl ko tác dụng được với Cu

a)
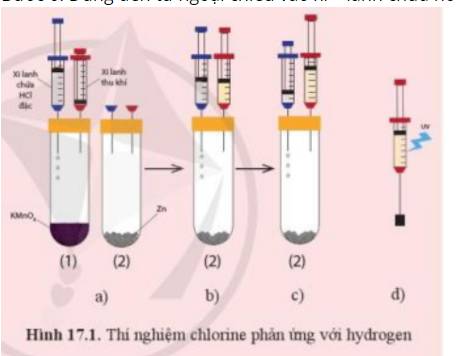
- Ở Bước 2: Ta thu được khí chlorine
- Ở Bước 4: Ta thu được khí hydrogen
=> Trong xi – lanh là hỗn hợp kí chlorine và hydrogen
- Khi chiếu đèn tử ngoại vào xi – lanh hoặc dùng ngọn lửa hơ nhẹ bên ngoài xi - lanh chứa hỗn hợp khí chlorine và hydrogen sẽ gây ra hiện tượng nổ
- Phương trình hóa học: H2 + Cl2 → 2HCl
b) Nếu thay khí chlorine bằng hơi iodine thì phản ứng giữa hơi iodine và hydrogen không xảy ra hiện tượng như trên.
- Giải thích: Phản ứng giữa H2 và I2 cần đun nóng để phản ứng diễn ra, là phản ứng thuận nghịch, tạo hỗn hợp gồm HI sinh ra và lượng H2, I2 còn lại. Khả năng phản ứng kém nên không có hiện tượng nổ
H2 + I2 \( \rightleftharpoons \) 2HI

Đáp án D
Phương trình phản ứng: Na 2 S 2 O 3 + H 2 SO 4 → Na 2 SO 4 + S ↓ + SO 2 ↑ + H 2 O
Nồng độ các chất phản ứng là Na2S2O3 và H2SO4 không đổi, do đó tốc độ phản ứng chỉ phụ thuộc nhiệt độ. Khi nhiệt độ tăng, tốc độ phản ứng tăng và thời gian phản ứng giảm.
Nhiệt độ ở các thí nghiệm tăng theo thứ tự sau: thí nghiệm 1 < thí nghiệm 3 < thí nghiệm 2, do đó tốc độ phản ứng thí nghiệm 1 < thí nghiệm 3 < thí nghiệm 2 và thời gian phản ứng thí nghiệm 1 > thí nghiệm 3 > thí nghiệm 2 => t 1 > t 3 > t 2 .

Đáp án D
Phương trình phản ứng: Na 2 S 2 O 3 + H 2 SO 4 → Na 2 SO 4 + S ↓ + SO 2 ↑ + H 2 O
Nồng độ chất tham gia phản ứng càng cao (nồng độ các chất trong dung dịch hỗn hợp khi trộn các chất với nhau), tốc độ phản ứng càng nhanh, thời gian kết tủa càng ngắn.
Ở đây, nồng độ dung dịch H2SO4 được giữ cố định (1 giọt), do đó trong dung dịch hỗn hợp thu được nồng độ H2SO4 không đổi, dẫn đến tốc độ phản ứng chỉ còn phụ thuộc vào nồng độ Na2S2O3.
Thứ tự tăng nồng độ Na2S2O3 trong các thí nghiệm sau: thí nghiệm 2 (12 giọt Na2S2O3 + 0 giọt H2O) > thí nghiệm 3 (8 giọt Na2S2O3 + 4 giọt H2O) > thí nghiệm 1 (4 giọt Na2S2O3 + 8 giọt H2O).
Vậy thời gian xuất hiện kết tủa theo thứ tự là t 1 > t 3 > t 2 .


Chọn C
Khối lượng HCl có trong dung dịch ở ống (1) là 3.18% = 0,54 gam.
Khối lượng HCl có trong dung dịch ở ống (2) là 9.6% = 0,54 gam.
C sai vì thể tích khí H2 (đo cùng điều kiện) thu được ở hai ống là như nhau.