Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



Qui đổi ½ hh B gồm Al (x mol), Fe (y mol), O (z mol)

=> mB = 2 (mAl + mFe + mO) = 102,78g
Gọi công thức của oxit sắt là FeaOb

=> Fe2O3

a) PTHH: 2Al + 6 HCl -> 2 AlCl3 + 3 H2
x___________3x______________1,5x(mol)
Fe +2 HCl -> FeCl2 + H2
y___2y____y______y(mol)
b) Ta có: m(rắn)= mCu=0,4(g)
=> m(Al, Fe)=1,5-mCu=1,5-0,4=1,1(g)
nH2= 0,04(mol)
Ta lập hpt:
\(\left\{{}\begin{matrix}27x+56y=1,1\\1,5x+y=0,04\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,02\\y=0,01\end{matrix}\right.\)
=> mAl=27.0,02=0,54(g)
mFe=56.0,01=0,56(g)

1.
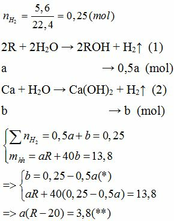
Vì b > 0, từ (*) => a < 0,25/0,5 = 0,5 thế vào (**)
=> R – 20 > 7,6
=> R > 27,6 (***)
Khi cho 8,58 gam R tác dụng với lượng dư HCl thì lượng H2 thoát ra lớn hơn 2,24 (lít)
2R + 2HCl → 2RCl + H2↑ (3)
Theo PTHH (3):
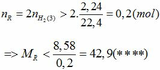
Từ (***) và (****) => 27, 6 < MR < 42,9
Vậy MR = 39 (K) thỏa mãn
2.
Ta có:
=> nKOH = nK = 0,2 (mol)
nCa(OH)2 = nCa = 0,15 (mol)
∑ nOH- = nKOH + 2nCa(OH)2 = 0,2 + 2.0,15 = 0,5 (mol)
Khi cho hỗn hợp Z ( N2, CO2) vào hỗn hợp Y chỉ có CO2 phản ứng
CO2 + OH- → HCO3- (3)
CO2 + 2OH- → CO32- + H2O (4)
CO32- + Ca2+ → CaCO3↓ (5)
nCaCO3 = 8,5/100 = 0,085 (mol) => nCO32-(5) = nCaCO3 = 0,085 (mol)
Ta thấy nCaCO3 < nCa2+ => phương trình (5) Ca2+ dư, CO32- phản ứng hết
TH1: CO2 tác dụng với OH- chỉ xảy ra phản ứng (4)
Theo (4) => nCO2 = nCO32-(4) = nCaCO3 = 0,085 (mol)
=> VCO2(đktc) = 0,085.22,4 = 1,904 (lít)
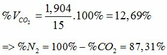
TH2: CO2 tác dụng với OH- xảy ra cả phương trình (3) và (4)
Theo (4): nCO2 = nCO32- = 0,085 (mol)
nOH- (4) = 2nCO32- = 2. 0,085 = 0,17 (mol)
=> nOH- (3)= ∑ nOH- - nOH-(4) = 0,5 – 0,17 = 0,33 (mol)
Theo PTHH (3): nCO2(3) = nOH- = 0,33 (mol)
=> ∑ nCO2(3+4) = 0,085 + 0,33 = 0,415 (mol)
=> VCO2 (ĐKTC) = 0,415.22,4 = 9,296 (lít)
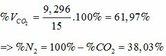

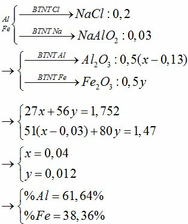



Câu 1 :
\(2NaHCO_3\rightarrow Na_2CO_3+H_2O+CO_2\)
\(Ca\left(HCO_3\right)_2\rightarrow CaCO_3+H_2O+CO_2\)
\(CaCO_3\rightarrow CaO+CO_2\)
\(Na_2CO_3+2HCl\rightarrow2NaCl+CO_2+H_2O\)
\(CaO+2HCl\rightarrow CaCl_2+H_2O\)
Ta có :
\(n_{CO2}=\frac{2,24}{22,4}=0,1\left(mol\right)\)
Gọi số mol NaHCO3: xmol ; Ca(HCO3)2: y mol
Giải hệ phương trình :
\(\left\{{}\begin{matrix}53x+56y=16,2\\\frac{1}{2}x=0,1\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,2\\y=0,1\end{matrix}\right.\)
\(\Rightarrow\%m_{NaHCO3}=\frac{0,2.72}{0,2.72+0,1.162}.100\%=47,06\%\)
\(\Rightarrow\%_{Ca\left(HCO_3\right)2}=100\%-47,06\%=52,94\%\)
Bài 2 :
\(Na_2CO_3+CaCl_2\rightarrow2NaCl+CaCO_3\)
\(n_{Na2CO3}=\frac{5,3}{160}=0,05\left(mol\right)\)
\(n_{CO2}=\frac{1,5.60\%}{22,4}=0,04\left(mol\right)\)
\(n_{CaCl2}=\frac{200.3\%}{111}=0,054\left(mol\right)\)
\(CaCO_3+CO_2+H_2O\rightarrow Ca\left(HCO_3\right)_2\)
\(n_{CaCO3}=0,05-0,04=0,01\left(mol\right)\)
\(\Rightarrow m_{CaCO3}=0,01.100=1\left(g\right)\)