Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) PTHH: \(3Fe+2O_2\underrightarrow{t^0}Fe_3O_4\left(1\right)\)
Ta có: \(n_{Fe_3O_4}=\dfrac{6,96}{232}=0,03\left(mol\right)\)
\(\Rightarrow n_{O_2}=2.0,03=0,06\left(mol\right)\)
\(\Rightarrow n_{Fe}=3.0,03=0,09\left(mol\right)\)
\(\Rightarrow m_{Fe}=0,09.56=5,04\left(mol\right)\)
b) PTHH: \(2KMnO_4\underrightarrow{t^0}K_2MnO_4+MnO_2+O_2\)
Ta có: \(n_{O_2\left(2\right)}=n_{O_2\left(1\right)}=0,06\left(mol\right)\)
\(\Rightarrow n_{KMnO_4}=2.0,06=0,12\left(mol\right)\)
\(\Rightarrow m_{KMnO_4}=0,12.158=18,96\left(g\right)\)

\(a/n_{Fe}=\dfrac{2,52}{56}=0,045mol\\ 3Fe+2O_2\xrightarrow[]{t^0}Fe_3O_4\\ n_{O_2}=\dfrac{0,045.2}{3}=0,03mol\\ V_{O_2}=0,03.22,4=0,672l\\ b/2KClO_3\xrightarrow[]{t^0}2KCl+3O_2\\ n_{KClO_3}=\dfrac{0,03.2}{3}=0,02mol\\ m_{KClO_3}=0,02.122,5=2,45g\)

\(n_{Fe_3O_4}=\dfrac{23,2}{232}=0,1mol\)
\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
0,3 0,2 0,1
\(V_{O_2}=0,2\cdot22,4=4,48l\)
\(n_{Fe_3O_4}=\dfrac{23,2}{232}=0,1mol\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
0,2 0,1 ( mol )
\(V_{O_2}=0,2.22,4=4,48l\)

nFe3O4 = \(\dfrac{2,32}{232}=0,01\) mol
Pt: 3Fe + ...2O2 --to--> Fe3O4
0,03 mol<-0,02 mol<--0,01 mol
mFe cần dùng = 0,03 . 56 = 1,68 (g)
VO2 cần dùng = 0,02 . 22,4 = 0,448 (lít)
Pt: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
...0,04 mol<---------------------------------0,02 mol
mKMnO4 cần dùng = 0,04 . 158 = 6,32 (g)
a) Theo đề bài ta có: \(n_{Fe_3O_4}=\dfrac{2,32}{232}=0,01\left(mol\right)\)
PTHH: \(3Fe+2O_2\underrightarrow{t^0}Fe_3O_4\)
0,03mol..........0,02mol.....0,01mol
\(\Rightarrow\left\{{}\begin{matrix}V_{O_2\left(đktc\right)}=0,02.22,4=0,448\left(l\right)\\V_{O_2\left(đktc\right)}=0,2.22=0,48\left(l\right)\end{matrix}\right.\)
\(\Rightarrow m_{Fe}=0,03.56=1,68\left(g\right)\)
b) PTHH:
\(2KMnO_4\underrightarrow{t^0}K2MnO_4+MnO_4+O_2\uparrow\)
0,04mol.................................0,02mol
\(\Rightarrow m_{KMnO_4}=0,04.158=6,32\left(g\right)\)

PTHH: \(2KMnO_4\xrightarrow[]{t^o}K_2MnO_4+MnO_2+O_2\uparrow\)
Ta có: \(n_{KMnO_4}=2n_{O_2}=2\cdot\dfrac{5,6}{22,4}=0,5\left(mol\right)\)
\(\Rightarrow m_{KMnO_4}=0,5\cdot158=79\left(g\right)\)

Sửa đề: Khối lượng kim loại thu được là bao nhiêu ?
Ta thấy Oxi trong oxit sẽ chuyển vào H2O
\(\Rightarrow n_O=n_{H_2O}=\dfrac{1}{2}HCl=\dfrac{1}{2}\cdot0,09=0,045\left(mol\right)\)
Mặt khác, khối lượng kim loại sau khi khử bằng CO hay khối lượng kim loại trong hh ban đầu là như nhau
\(\Rightarrow m_{kim.loại}=m_{hh}-m_O=5,44-0,045\cdot16=4,72\left(g\right)\)

a) Các phương trình phản ứng
2KNO3 2KNO2 + O2↑ (1)
2KClO3 2KCl + 3O2↑ (2)
b) Theo (1) và (2), thấy số mol hai muối tham gia phản ứng như nhau nhưng số mol oxi tạo thành khác nhau và do đó thể tích khí oxi thu được là khác nhau.
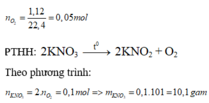
Theo (1): nO2 = nKNO3 =
= 0,05 mol; VO2 = 0,05x22,4 = 1,12 lít
Theo (2): nO2 = nKClO3 =
= 0,15 mol; VO2 = 0,15x22,4 = 3,36 lít
c) Để thu được 1,12 lít khí (0,05 mol) O2, thì:
Theo (1): nKNO3 = 2nO2 = = 0,1 mol; mKNO3 = 0,1x101 = 10,1 g
Theo (2): nKClO3 = nO2 =
x0,05 mol; VKClO3 =
x0,05x122,5 = 4,086 g.

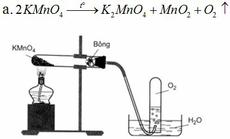
b.
Rắn A gồm: KMnO4, K2MnO4, MnO2
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 ↑+ 8H2O
K2MnO4 + 8HCl → 2KCl + MnCl2 + 2Cl2↑ + 4H2O
MnO2 + 4HCl → MnCl2 + Cl2↑ + 2H2O
Vậy khí B là Cl2.
PTHH: \(3Fe+2O_2\xrightarrow[]{t^o}Fe_3O_4\)
Ta có; \(n_{Fe_3O_4}=\dfrac{2,32}{232}=0,01\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Fe}=0,03\left(mol\right)\\n_{O_2}=0,02\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Fe}=0,03\cdot56=1,68\left(g\right)\\V_{O_2}=0,02\cdot22,4=0,448\left(l\right)\end{matrix}\right.\)