A là hỗn hợp gồm Ba, Al, Mg. Lấy M gam A cho tác dụng với nước tới khi hết phản ứng thấy thoát ra 3,7185 lít khí H2 ở (ĐKC). lây M gam A cho vào dung dịch NaOH dư tới khi hết phản ứng thấy thoát ra 7,437 khí H2 ở (ĐKC). lấy M gam A hòa tan bằng 1 lượng vừa đủ acid HCL thì thu được 1 đ và 9,916 lít H2 ở (ĐKC). hãy tính gam và thành phần phần trăm theo khối lượng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

đáp án của bài theo quận hơi kì đó là :m=24,65g
mBa=19,55g
mAl=2,7g
mMg=2,4g
trong khi em ra mHH:= 12,2625g %mBa:=42% %mAl=38,5% %mMg=19,5%
mong mọi người giúp ạ

Gọi số mol của Ba, Al và Mg lần lượt là x, y và z mol
Lượng khí thu được khi cho A vào nước dư ít hơn khi cho A vào xút dư nên khi cho A vào nước dư thì Ba phản ứng hết, Al phản ứng một phần. Khi cho A vào xút dư thì cả Ba và Al đều phản ứng hết.
Cho A tác dụng với nước dư có phản ứng:
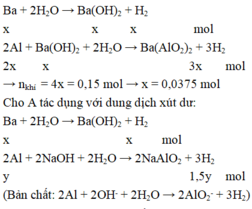

Khối lượng của A là: m = 0,0375.137 + 0,175.27 + 0,1.24 = 12,2625 gam.
⇒ Chọn B

TN1: A tác dụng với nước
Ba +2 H2O --> Ba(OH)2 + H2;
x ------------------x------------x ;
2Al + Ba(OH)2 +2 H2O --> Ba(AlO2)2 +3 H2;
2x--------x---------------------------------------3x;
TN2 : A tác dụng với dd xút
Ba +2 H2O --> Ba(OH)2 + H2;
x----------------------------------x;
2Al + Ba(OH)2 +2 H2O --> Ba(AlO2)2 +3 H2;
y-------------------------------------------------3/2y;
TN3: A tác dụng với HCl
Ba + 2HCl --> BaCl2 + H2;
x------------------------------x;
2Al + 6HCl --> 2AlCl3 + 3H2;
y------------------------------3/2y;
Mg + 2HCl --> MgCl2 + H2;
z------------------------------z;
Gọi x,y,z lần lượt là số mol của Ba, Al, Mg.
TN1: nH2= 3,36/22,4= 0,15 (mol)
=>x + 3x= 4x=0,15 => x= 0,0375 (mol)
TN2: nH2= 0,3 (mol)
=> x + 3/2 y = 0,3 => y = 0,175 (mol)
TN3: nH2= 0,4 (mol)
=> x +3/2y + z = 0,4 => Z= 0,1 (mol)
m= 0,0375*137+ 0,175*27+ 0,1*24=26,2625(g).

Khi cho A vào H2O và khi cho A vào NaOH thể tích khí thoát ra khác ở TN1 bé hơn chứng tỏ trong TN1 Al dư, vậy nH2 = 0,04 mol = 4nBa => nBa = 0,01 mol
Ba + H2O ------> Ba(OH)2 + H2
Al + OH- + H2O -----> AlO2- + 3/2 H2
nOH- = 2nBa
nH2 = nBa + 3/2.2nBa = 4nBa
nH2 ở TN2 = 0,31 mol = nBa + 3/2 nAl ( Vì OH- dư)
=> nAl = 0,2 mol
nH2 ở TN3 = 0,41 mol = nBa + 3/2nAl + nMg
=> nMg = 0,1 mol
Al + 3HCl -----> AlCl3 + 3/2H2
Mg + HCl -------> MgCl2 + H2
1. m = 21,5 gam
%Ba = 0,1.137/ 21,5.100 = 63,72%
%Al = 0,2.27/ 21,5.100 = 25,12%
%Mg = 100 -25,12 - 63,62 = 11,16%

HD:
Thí nghiệm 1 chỉ có Na phản ứng:
Na + HOH \(\rightarrow\) NaOH + 1/2H2 (1)
0,4 0,2 mol
Thí nghiệm 2 chỉ có Al phản ứng (kim loại lưỡng tính):
Al + OH- + H2O \(\rightarrow\) AlO2- + 3/2H2 (2)
0,7/3 0,35 mol
Thí nghiệm 3 cả 3 chất đều phản ứng:
2Na + H2SO4 \(\rightarrow\) Na2SO4 + H2 (3)
Mg + H2SO4 \(\rightarrow\) MgSO4 + H2 (4)
2Al + 3H2SO4 \(\rightarrow\) Al2(SO4)3 + 3H2 (5)
Gọi x, y, z tương ứng là số mol của Na, Mg và Al trong a gam hh.
Ta có: x = 0,4 mol; z = 0,7/3 mol; x/2 + y + 3z/2 = 0,5. Suy ra: y = -0.5 < 0 (vô lí)
Bạn xem lại đề bài, đề bài ko đúng.

Tính số mol KHSO4 = BaSO4 = 1,53 mol
→Fe(NO3)3 =0,035 mol
Hai khí còn lại là NO và N2O, số mol là x, y.
Lập hệ phương trình về tổng khối lượng và số mol tìm được x = 0,01 và y = 0,02.
Bảo toàn N tính số mol NH4+ = 0,025 mol
Bảo toàn H tính số mol H2O = 0,675 mol
Bảo toàn O:
![]()
Suy ra nO (B) = 0,4 ⟶ mB = 6,4:64 / 205 = 20,5g
Đáp án B

Đáp án D
n h h k h i = 0 , 2 m o l
cho BaCl2 vào kết tủa thu được là BaSO4
n B a S O 4 = 0 , 605 m o l
n H 2 S O 4 = 0 , 605 m o l
n N a O H = 1 , 085 m o l
n N H 3 = 0 , 025 m o l
⇒ n i o n k i m l o a i = 1 , 06 m o l
hỗn hợp khí có chứa H2 nên muối sắt là muối Fe2+
NO3- hết, các muối trung hòa là
MgSO4, FeSO4, K2SO4 và (NH4)2SO4
m F e + m M g = 24,88 gam (1)
nđiện tích - = 2nSO42-= 1,21 mol
nđiện tích += 1,085 + n K +
=> n K + = 0,125 mol
=>nN khí = 0,125 – 0,025 =0,1 mol
Mặt khác bảo toàn khối lượng
m X + m H 2 S O 4 + m K N O 3 = m m u ố i + m k h í + m H 2 O
=> m H 2 O = 8,91 mol
=> n H 2 O = 0,495 mol
Bảo toàn nguyên tố H có
nH axit = nH ( H 2 O )+ nH ( H 2 ) +nH muối amoni
0,605.2 =0,495.2 +2 n H 2 + 0,025.4
=> n H 2 = 0,06 mol
=> n C O 2 = 0,2 – 0,1 – 0,06 = 0,04 mol
=> n F e C O 3 = 0,04 mol
=> mFe + mMg + m F e 3 O 4 = 26,48 g
m KL (hỗn hợp trên)= 22,64 gam (2)
từ (1) và (2) => mO ( F e 3 O 4 )= 3,84 gam
=> n F e 3 O 4 =0,06 mol
mặt khác vì tổng ion dương kim loại F e 2 + v à M g 2 +
Gọi n F e = a m o l , n M g = b m o l
⇒ 2 a + 2 b = 0 , 2 56 a + 24 b = 12 , 56
⇒ a = 0 , 16 , b = 0 , 15 m o l



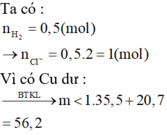
A tác dụng với nước
\(n_{H_2}=\dfrac{3,7185}{24,79}=0,15mol\\ Ba+2H_2O\rightarrow Ba\left(OH\right)_2+H_2\)
\(a----------\rightarrow a\)
\(Ba\left(OH\right)_2+2Al+2H_2O\rightarrow Ba\left(AlO_2\right)_2+3H_2\)
\(a----------------\rightarrow3a\)
\(\Rightarrow a+3a=0,15\\ \Rightarrow a=0,0375mol\)
A tác dụng với NaOH
\(n_{H_2}=\dfrac{7,347}{24,79}=0,3mol\)
\(Ba+2H_2O\rightarrow Ba\left(OH\right)_2+H_2\)
\(a----------\rightarrow a\)
\(2Al+2NaOH+2H_2O\rightarrow2NaAlO_2+3H_2\)
\(b---------------\rightarrow1,5b\)
\(\Rightarrow a+1,5b=0,3\\ \Rightarrow0,0375+1,5b=0,3\\ \Rightarrow b=0,175mol\)
A tác dụng với HCl
\(n_{H_2}=\dfrac{9,916}{24,79}=0,4mol\)
\(Ba+2HCl\rightarrow BaCl_2+H_2\)
\(a---------\rightarrow a\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(b---------\rightarrow1,5b\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(c---------\rightarrow c\)
\(\Rightarrow a+1,5b+c=0,4\\ \Rightarrow0,0375+1,5.0,175+c=0,4\\ \Rightarrow c=0,1mol\)
\(m_A=0,0375.137+0,175.27+0,1.24=12,2625g\\ \%m_{Ba}=\dfrac{0,0375.137}{12,2625}\cdot100=41,9\%\\ \%m_{Al}=\dfrac{0,175.27}{12,2625}\cdot100=38,53\%\\ \%m_{Mg}=100-41,9-38,53=19,57\%\)