Tính phi kim được đặc trưng bằng khả năng nhận electron. Xu hướng cơ bản của nguyên tử O và F trong các phản ứng hóa học là nhường hay nhận bao nhiêu electron.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


- Cấu hình nguyên tử nitrogen (Z = 7): 1s22s22p3
=> Có 5 electron ở lớp vỏ ngoài cùng => Có xu hướng nhận thêm 3 electron để đạt cấu hình electron khí hiếm
- Cấu hình nguyên tử nhôm (Z = 13): 1s22s22p63s23p1
=> Có 3 electron ở lớp vỏ ngoài cùng => Có xu hướng nhường đi 3 electron để đạt cấu hình electron khí hiếm
Đáp án A

Để chuyển thành anion mang điện tích âm, nguyên tử của các nguyên tố nhóm halogen nhận thêm electron (do có 7 e lớp ngoài cùng).

Cấu hình electron của nguyên tử S (Z = 16): 1s22s22p63s23p4. Để đạt cấu hình electron của khí hiếm gần nhất (Ar) trong Bảng tuần hoàn nguyên tử S nhận 2 electron để đạt 8e ở lớp ngoài cùng. S có tính phi kim.
S + 2e → S2-

a)
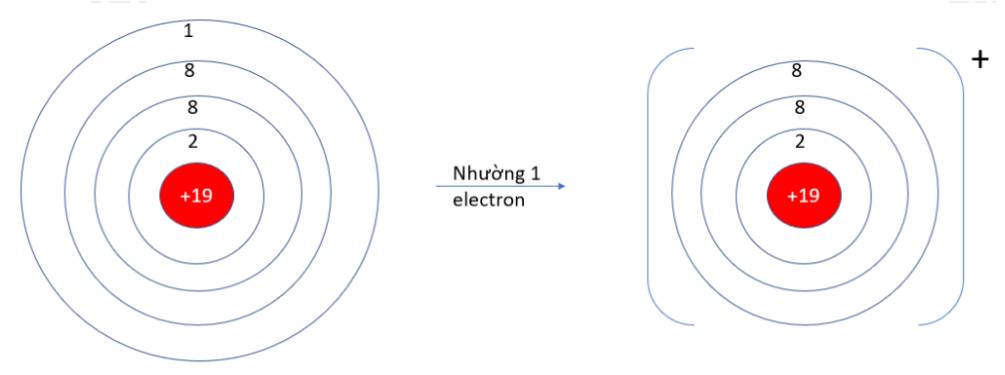
- K (Z = 19): 1s22s22p63s23p64s1 => Có 1 electron ở lớp vỏ ngoài cùng => Xu hướng nhường 1 electron
- O (Z = 8): 1s22s22p4 => Có 6 electron ở lớp vỏ ngoài cùng => Xu hướng nhận 2 electron

b)
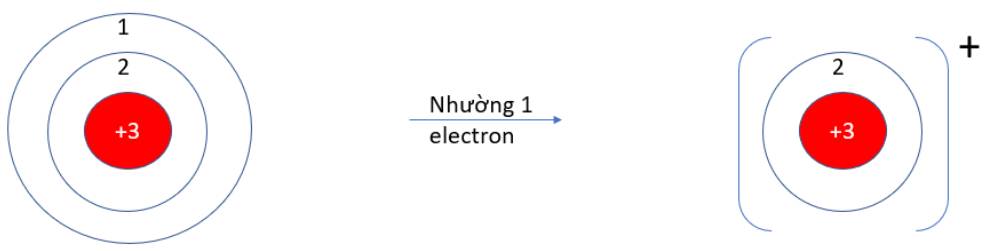
- Li (Z = 3): 1s22s1 => Có 1 electron ở lớp vỏ ngoài cùng => Xu hướng nhường 1 electron
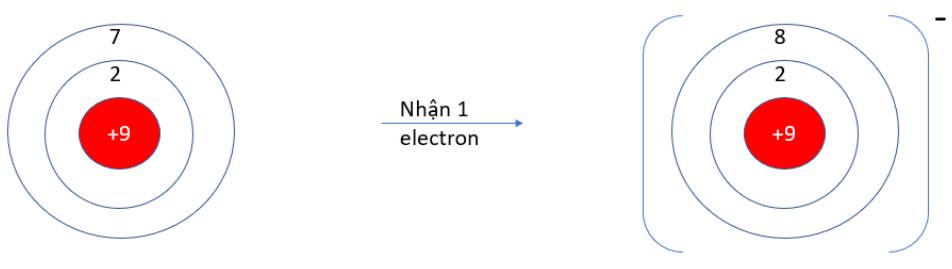
- F (Z = 9): 1s22s22p5 => Có 7 electron ở lớp vỏ ngoài cùng => Xu hướng nhận 1 electron
c)
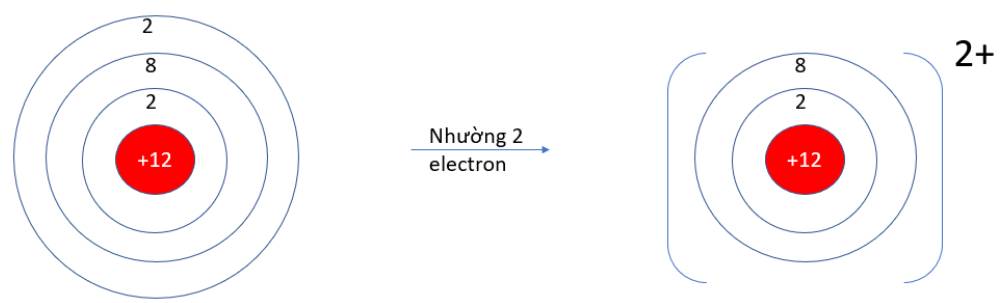
- Mg (Z = 12): 1s22s22p63s2 => Có 2 electron ở lớp vỏ ngoài cùng => Xu hướng nhường 2 electron
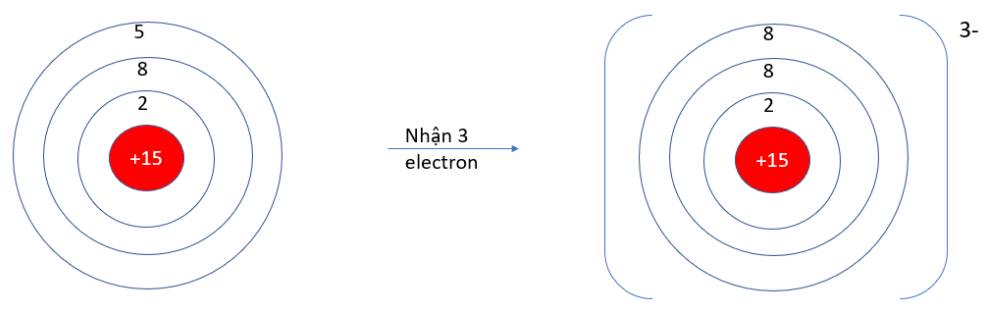
- P (Z = 15): 1s22s22p63s23p3 => Có 5 electron ở lớp vỏ ngoài cùng => Xu hướng nhận 3 electron

Chọn đáp án A
Các nguyên tử nguyên tố halogen có 7 electron ở lớp ngoài cùng. Để đạt cấu hình electron bền vững của khí hiếm, chúng dễ nhận thêm 1e để tạo thành anion.

Liti mất 1e (3 – 1 = 2) lớp ngoài cùng nên ion Li mang điện tích +1
Nito thêm 3e (5 + 3 = 8) lớp ngoài cùng nên ion N mang điện tích –5 (N–5)
Công thức phân tử Li3N

Cấu hình electron của nguyên tử Mg (Z = 12) : 1s22s22p63s2. Để đạt cấu hình electron của khí hiếm gần nhất (Ne) trong Bảng tuần hoàn nguyên tử Mg nhường 2 electron để đạt 8e ở lớp ngoài cùng. Mg có tính kim loại.
Mg – 2e → Mg2+

- Ta có: O và F đều là phi kim => Xu hướng cơ bản của nguyên tử O và F trong phản ứng hóa học là nhận electron
- Cấu hình electron O (Z = 8): 1s22s22p4 => Có 6 electron ở lớp vỏ ngoài cùng => Xu hướng nhận 2 electron
- Cấu hình electron F (Z = 9): 1s22s22p5=> Có 7 electron ở lớp vỏ ngoài cùng => Xu hướng nhận 1 electron