Hoàn thành các phương trình hoá học của các phản ứng sau:
a) (CH3)2CHCOOH + Ca →
b) HOOC – COOH + NaOH →
c) HCOOH + Na2CO3 →
d) C2H5COOH + CuO →
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Các phản ứng a,b,c là các phản ứng trùng hợp; d,e là các phản ứng trùng ngưng
a. nCH3-CH=CH2 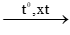
b. nCH2=CCl-CH=CH2 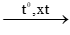
c. nCH2=C(CH3)-CH=CH2 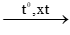
d. nCH2OH-CH2 OH + m-HOOC-C6H4-COOH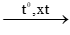
e. nNH2-[CH2]10-COOH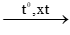

a) HCHO + 4(Ag(NH3)2)OH (NH4)2CO3 +4Ag + 6NH3 + 2H2O
b) C2H5CHO + Cu(OH)2 + NaOH C2H5COONa + Cu2O + 3H2O
c) C2H5CH=O + HCN → C2H5-CH(CN)-OH

I)
1) CuO + CO --to--> Cu + CO2
2) CO2 + Ca(OH)2 ---> CaCO3 + H2O
3) NaHCO3 + NaOH ---> Na2CO3 + H2O
4) Ca(HCO3)2 + 2KOH ---> CaCO3 + K2CO3 + 2H2O
II) \(n_{H_3PO_4}=0,05.1=0,05\left(mol\right)\)
PTHH: 2NaOH + H3PO4 ---> Na2HPO4 + 2H2O
0,1<----0,05--------->0,5
=> \(\left\{{}\begin{matrix}V=V_{ddNaOH}=\dfrac{0,1}{1}=0,1\left(l\right)=100\left(ml\right)\\m_{muối}=m_{Na_2HPO_4}=0,05.142=7,1\left(g\right)\end{matrix}\right.\)
III)
| NH4Cl | NaNO3 | NaBr | Cu(NO3)2 | |
| dd AgNO3 | - Kết tủa trắng | - Không hiện tượng | - Kết tủa vàng nhạt | - Không hiện tượng |
| dd NaOH | - Không hiện tượng | - Kết tủa xanh lơ |
NH4Cl + AgNO3 ---> AgCl + NH4NO3
NaBr + AgNO3 ---> AgBr + NaNO3
Cu(NO3)2 + 2NaOH ---> Cu(OH)2 + 2NaNO3
IV)
Gọi nCu = a (mol); nAl = b (mol)
=> 64a + 27b = 15 (1)
\(n_{NO}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Quá trình oxi hóa, khử:
Cu0 ---> Cu+2 + 2e
a---------------->2a
Al0 ---> Al+3 + 3e
b--------------->3b
N+5 + 3e ---> N+2
0,9<----0,9
BTe: 2a + 3b = 0,9 (2)
Từ (1), (2) => a = 0,15; b = 0,2
=> \(\left\{{}\begin{matrix}\%m_{Cu}=\dfrac{0,15.64}{15}.100\%=64\%\\\%m_{Al}=100\%-64\%=36\%\end{matrix}\right.\)

1.
a. \(Mg+CuSO_4\rightarrow MgSO_4+Cu\)
b. \(ZnCl_2+2NaOH\rightarrow Zn\left(OH\right)_2+2NaCl\)
c. \(Na_2CO_3+2HCl\rightarrow2NaCl+CO_2+H_2O\)
d. \(2Al\left(OH\right)_3\underrightarrow{t^o}Al_2O_3+3H_2O\)
2.
a.
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
0,2 0,2 0,2 0,2
Cu không pứ với \(H_2SO_{4.\left(loãng\right)}\)
b.
Từ pthh suy ra: \(\%_{m_{Fe}}=\dfrac{0,2.56.100}{17,6}=63,64\%\)
=> \(\%_{m_{Cu}}=100-63,64=36,36\%\)
c. dd sau pứ: FeSO4
có: \(m_{hh}+m_{dd.axit}-m_{H_2}=17,6+239,2-0,2.2=256,4\left(g\right)\)
=> \(C\%_{FeSO_4}=\dfrac{0,2.152.100}{256,4}=11,86\%\)

$1) HCOOH + CH_3OH \buildrel{{H_2SO_4,t^o}}\over\rightleftharpoons + HCOOCH_3 + H_2O$
$2) CH_3-CH_2-COOH + CH_3OH \buildrel{{H_2SO_4,t^o}}\over\rightleftharpoons CH_3-CH_2-COOCH_3 + H_2O$
$3) CH_2=CH-COOH + CH_3OH \buildrel{{H_2SO_4,t^o}}\over\rightleftharpoons CH_2=CH-COOCH_3 + H_2O$
$4) CH_3COOH + C_2H_5OH \buildrel{{H_2SO_4,t^o}}\over\rightleftharpoons CH_3COOC_2H_5 + H_2O$
$5) CH_3-CH_2-COOH + CH_3OH \buildrel{{H_2SO_4,t^o}}\over\rightleftharpoons CH_3-CH_2-COOCH_3 + H_2O$
$6) HCOOH + CH_3-CH_2-CH_2-OH \buildrel{{H_2SO_4,t^o}}\over\rightleftharpoons HCOOCH_3-CH_2-CH_3 + H_2O$
$7) CH_3COOH + CH≡CH \buildrel{{H_2SO_4,t^o}}\over\rightleftharpoons CH_3COOCH=CH_2$
$8) CH_3COOH + C_6H_5CH_2OH \buildrel{{H_2SO_4,t^o}}\over\rightleftharpoons CH_3COOCH_2C_6H_5 + H_2O$
$9) CH_3-CH_2-COOH + CH_3OH \buildrel{{H_2SO_4,t^o}}\over\rightleftharpoons CH_3-CH_2-COOCH_3 + H_2O$
$10) CH_2=CH-COOH + C_2H_5OH \buildrel{{H_2SO_4,t^o}}\over\rightleftharpoons CH_2=CH-COOC_2H_5 + H_2O$

Đáp án B
Hướng dẫn
Nhóm ankyl đẩy e làm cho tính axit giảm, nhóm ankyl càng lớn thì tính axit càng giảm.
(2) có 2 nhóm –CH3 đẩy e mạnh hơn nhóm CH3CH2CH2- nên tính axit của (5) mạnh hơn (2)
a) 2(CH3)2CHCOOH + Ca → 2((CH3)2CHCOO)2Ca + H2↑
b) HOOC-COOH + 2NaOH → NaOOC-COONa + 2H2O
c) 2HCOOH + Na2CO3 → 2HCOONa + H2O + CO2↑
d) 2C2H5COOH+CuO → (C2H5COO)2Cu + H2O