( 1,25 x y - y ) : 0,01 = 15 - 2,5
giúp em với ạ , em cần lời giải chi tiết . Cảm ơn.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

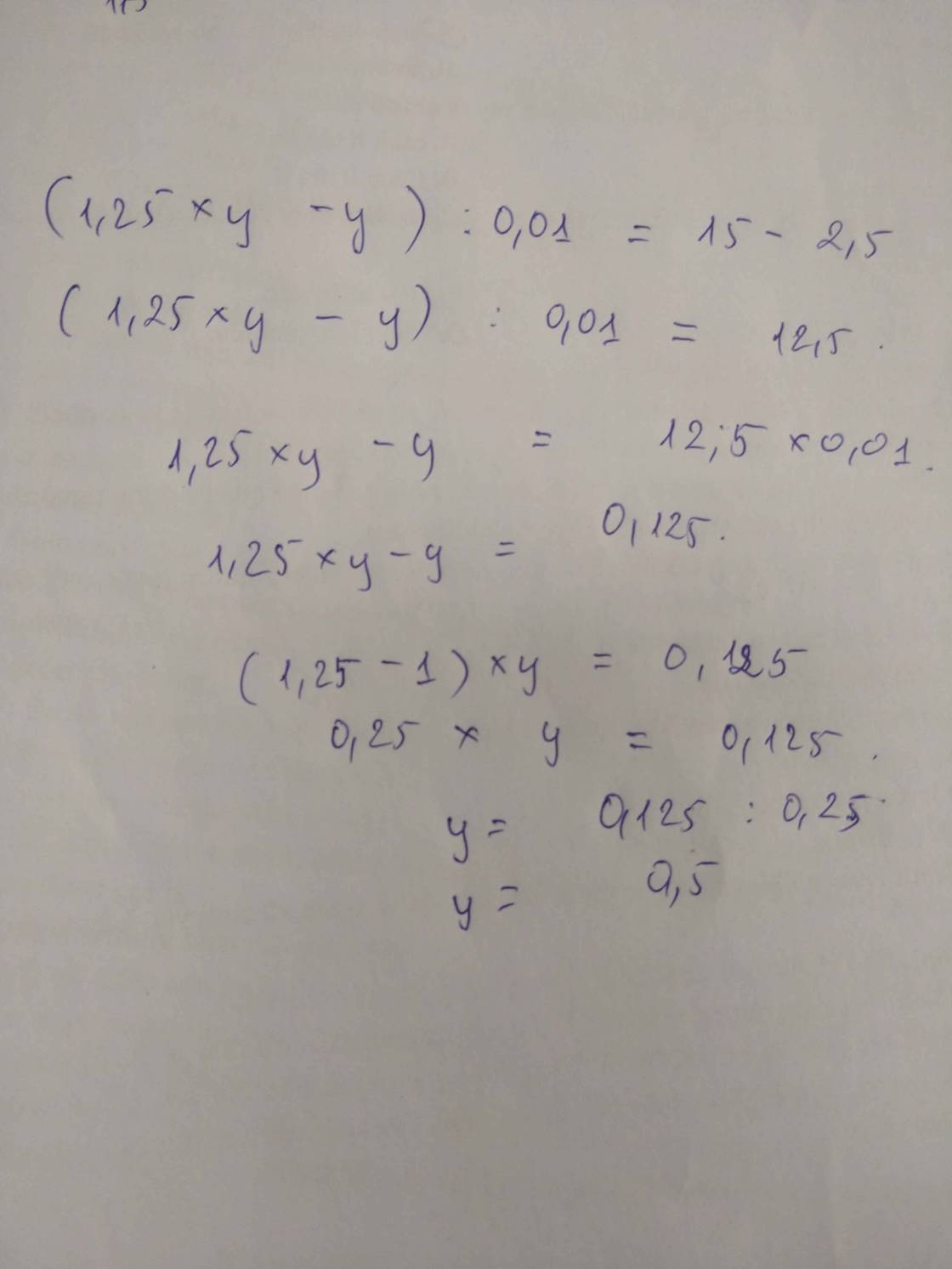


Khối lượng của hợp kim đó :
\(8,5:\dfrac{5}{8}=13,6\left(kg\right)\)


3.
\(4sinx+cosx+2cos\left(x+\dfrac{\pi}{3}\right)=2\)
\(\Leftrightarrow4sinx+cosx+cosx-\sqrt{3}sinx=2\)
\(\Leftrightarrow\left(4-\sqrt{3}\right)sinx+2cosx=2\)
\(\Leftrightarrow\sqrt{23-4\sqrt{3}}\left(\dfrac{4-\sqrt{3}}{\sqrt{23-4\sqrt{3}}}sinx+\dfrac{2}{\sqrt{23-4\sqrt{3}}}cosx\right)=2\)
\(\Leftrightarrow cos\left(x-arccos\dfrac{2}{\sqrt{23-4\sqrt{3}}}\right)=\dfrac{2}{\sqrt{23-4\sqrt{3}}}\)
\(\Leftrightarrow x-arccos\dfrac{2}{\sqrt{23-4\sqrt{3}}}=\pm arccos\dfrac{2}{\sqrt{23-4\sqrt{3}}}+k2\pi\)
\(\Leftrightarrow\left[{}\begin{matrix}x=2arccos\dfrac{2}{\sqrt{23-4\sqrt{3}}}+k2\pi\\x=k2\pi\end{matrix}\right.\)
4.
\(sinx+2cos\left(x+\dfrac{\pi}{3}\right)+4sin\left(x+\dfrac{\pi}{6}\right)+cosx=4\)
\(\Leftrightarrow sinx+cosx-\sqrt{3}sinx+2\sqrt{3}sinx+2cosx+cosx=4\)
\(\Leftrightarrow\left(1+\sqrt{3}\right)sinx+4cosx=4\)
\(\Leftrightarrow\sqrt{20+2\sqrt{3}}\left(\dfrac{1+\sqrt{3}}{\sqrt{20+2\sqrt{3}}}sinx+\dfrac{4}{\sqrt{20+2\sqrt{3}}}cosx\right)=4\)
\(\Leftrightarrow cos\left(x-arccos\dfrac{4}{\sqrt{20+2\sqrt{3}}}\right)=\dfrac{4}{\sqrt{20+2\sqrt{3}}}\)
\(\Leftrightarrow x-arccos\dfrac{4}{\sqrt{20+2\sqrt{3}}}=\pm arccos\dfrac{4}{\sqrt{20+2\sqrt{3}}}+k2\pi\)
\(\Leftrightarrow\left[{}\begin{matrix}x=2arccos\dfrac{4}{\sqrt{20+2\sqrt{3}}}+k2\pi\\x=k2\pi\end{matrix}\right.\)

Câu 40. \(n_{NaOH}=\dfrac{20}{40}=0,5\left(mol\right);n_{HCl}=\dfrac{36,5}{36,5}=1\left(mol\right)\)
PTHH: \(NaOH+HCl\rightarrow NaCl+H_2O\)
Theo đề: 0,5mol .....1mol
Lập tỉ lệ : \(\dfrac{0,5}{1}< \dfrac{1}{1}\)=> Sau phản ứng NaOH hết, HCl dư
=> Thử môi trường sau phản ứng bằng quỳ sẽ có màu đỏ
Câu 41.
nNaOH=0,3.0,5=0,15(mol);nHCl=0,3.1=0,3(mol)
PTHH: NaOH + HCl → NaCl + H2O
Theo đề:0,15mol ....0,3mol
Lập tỉ lệ :\(\dfrac{0,15}{1}< \dfrac{0,3}{1}\)=> Sau phản ứng NaOH hết, HCl dư
=> Dung dịch sau phản ứng làm quỳ tím hóa màu đỏ

\(\dfrac{x}{\dfrac{4}{2}}=\dfrac{4}{\dfrac{x}{2}}\)
\(\Rightarrow\dfrac{x}{2}=\dfrac{8}{x}\)
\(\Rightarrow x^2=8\cdot2\)
\(\Rightarrow x^2=16\)
\(\Rightarrow x^2=4^2\)
\(\Rightarrow\left[{}\begin{matrix}x=4\\x=-4\end{matrix}\right.\)

Lời giải:
\(H=2-\frac{3}{17}-\frac{5}{23}+\frac{2}{17}-\frac{1}{2023}-\frac{16}{17}-\frac{18}{23}\\ =2-(\frac{3}{17}-\frac{2}{17}+\frac{16}{17})-(\frac{5}{23}+\frac{18}{23})-\frac{1}{2023}\\ =2-1-1-\frac{1}{2023}=-\frac{1}{2023}\)
---------------------
\(K=\frac{7}{23}.\frac{-11}{17}+\frac{7}{23}.\frac{4}{17}-\frac{7}{23}.\frac{10}{17}\\ =\frac{7}{23}(\frac{-11}{17}+\frac{4}{17}-\frac{10}{17})\\ =\frac{7}{23}.\frac{-17}{17}=\frac{-7}{23}\)

\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\\ n_S=\dfrac{3,2}{32}=0,1\left(mol\right)\\ PTHH:Fe+S\underrightarrow{t^o}FeS\left(1\right)\\ LTL:0,2>0,1\Leftrightarrow Fe.dư\)
\(Theo.pt\left(1\right):n_{Fe\left(pư\right)}=n_{FeS}=0,1\left(mol\right)\\ n_{FeS\left(dư\right)}=0,2-0,1=0,1\left(mol\right)\)
\(PTHH:FeS+H_2SO_4\rightarrow FeSO_4+H_2S\uparrow\left(2\right)\\ Fe+2H_2SO_4\rightarrow FeSO_4+SO_2\uparrow+2H_2O\left(3\right)\)
\(Theo.pt\left(2\right):n_{H_2S}=n_{FeS}=0,1\left(mol\right)\\ Theo.pt\left(3\right):n_{SO_2}=n_{Fe}=0,1\left(mol\right)\\ \%V_{H_2S}=\dfrac{0,1}{0,1+0,1}=50\%\\ \%V_{SO_2}=100\%-50\%=50\%\)
\(Theo.pt\left(2\right):n_{H_2SO_4\left(2\right)}=n_{FeS}=0,1\left(mol\right)\\ Theo.pt\left(3\right):n_{H_2SO_4\left(3\right)}=2n_{Fe}=2.0,1=0,3\left(mol\right)\\ C_{MddH_2SO_4}=\dfrac{0,3}{0,2}=1,5M\)