Câu 5: Tính khối lượng nước để hòa tan vào dung dịch trong các trường hợp sau:
a/ Pha thêm vào 300g dung dịch H2SO4 19,6% để thu được dung dịch 9,8%.
b/ Pha thêm vào 200ml dung dịch HCl 2M thành dung dịch 1,5M
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án A
Câu này rất đơn giản dữ kiện 0,54 gam Al không cần thiết.Kết tủa lớn nhất khi Na trong NaOH chạy vào NaCl và Na2SO4
Ta có

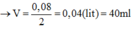

\(a.m_{ddNaCl}=\dfrac{15}{5}\cdot100=300g\\ b.m_{nước}+m_{muối}=m_{dd,muối}\\ \Rightarrow m_{nước}=m_{dd,muối}-m_{muối}\\ =300-15\\ =285g\)

1. \(n_{H_2SO_4\left(98\%\right)}=\dfrac{30.1,84.98\%}{98}=0,552\left(mol\right)\)
=>\(V_{H_2SO_4\left(1M\right)}=\dfrac{0,552}{1}=0,552\left(l\right)\)

\(n_{Na}=\dfrac{2.3}{23}=0.1\left(mol\right)\)
\(n_{HCl}=0.4\cdot2=0.8\left(mol\right)\)
\(NaOH+HCl\rightarrow NaCl+H_2O\)
\(0.8..............0.8\)
\(2Na+2H_2O\rightarrow2NaOH+H_{_{ }2}\)
\(0.1........................0.1\)
\(n_{NaOH}=0.1< 0.8\)
Đề nhầm lãn !

PTHH: \(Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\) (1)
\(HCl+NaOH\rightarrow NaCl+H_2O\) (2)
\(AlCl_3+3NaOH\rightarrow3NaCl+Al\left(OH\right)_3\downarrow\) (3)
Ta có: \(\left\{{}\begin{matrix}n_{Al_2O_3}=\dfrac{6,12}{102}=0,06\left(mol\right)\\\Sigma n_{HCl}=0,2\cdot2=0,4\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,06}{1}< \dfrac{0,4}{6}\) \(\Rightarrow\) HCl còn dư, Al2O3 p/ứ hết
Vì bazơ mạnh sẽ p/ứ với axit mạnh trước nên sẽ xảy ra p/ứ (2) và (3)
Lại có: \(n_{Al\left(OH\right)_3}=\dfrac{7,8}{78}=0,1\left(mol\right)=n_{AlCl_3\left(3\right)}\)
Theo PTHH (1): \(n_{AlCl_3\left(1\right)}=0,12\left(mol\right)\)
\(\Rightarrow\) AlCl3 còn dư nên tính theo Al(OH)3 \(\Rightarrow n_{NaOH\left(3\right)}=0,3\left(mol\right)\)
Mặt khác: \(n_{HCl\left(dư\right)}=n_{HCl\left(2\right)}=0,04\left(mol\right)=n_{NaOH\left(2\right)}\)
\(\Rightarrow\Sigma n_{NaOH}=0,34\left(mol\right)\) \(\Rightarrow V_{NaOH}=\dfrac{0,34}{2}=0,17\left(l\right)=170\left(ml\right)\)

Câu 1:
PT ion: \(H^++OH^-\rightarrow H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{OH^-}=0,6\cdot0,4+0,6\cdot0,3\cdot2=0,6\left(mol\right)\\n_{H^+}=0,2\cdot2,6=0,52\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\) H+ hết, OH- còn dư \(\Rightarrow n_{OH^-\left(dư\right)}=0,08\left(mol\right)\)
\(\Rightarrow\left[OH^-\right]=\dfrac{0,08}{0,6+0,2}=0,1\left(M\right)\) \(\Rightarrow pH=14+log\left(0,1\right)=13\)
Bài 2:
PT ion: \(H^++OH^-\rightarrow H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{OH^-}=0,3\cdot1,6=0,48\left(mol\right)\\n_{H^+}=0,2\cdot1\cdot2+0,2\cdot2=0,8\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\) OH- hết, H+ còn dư \(\Rightarrow n_{H^+\left(dư\right)}=0,32\left(mol\right)\)
\(\Rightarrow\left[H^+\right]=\dfrac{0,32}{0,2+0,3}=0,64\left(M\right)\) \(\Rightarrow pH=-log\left(0,64\right)\approx0,19\)

\(m_{NaOH\left(35\%\right)}=100.35\%=35\left(g\right)\)
\(m_{ddNaOH\left(20\%\right)}=\dfrac{35}{20}.100=175\left(g\right)\)
⇒ mnước thêm vào = 175-100 = 75(g)
Vnước thêm vào = 75.1 = 75 (ml)

\(a,m_{NaCl}=\dfrac{8.200}{100}=16\left(g\right)\\ b,m_{HCl}=\dfrac{250.14}{100}=35\left(g\right)\\ m_{H_2SO_4}=\dfrac{19,6.300}{100}=58,8\left(g\right)\)

\(n_{H_2SO_4}=\dfrac{19,6\%.500.1,12}{98}=1,12\left(mol\right)\\n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ MgO+H_2SO_4 \rightarrow MgSO_4+H_2O\\ CaCO_3+H_2SO_4\rightarrow CaSO_4+CO_2+H_2O\\ TH1:axit.hết\\ n_{CO_2}=n_{CaCO_3}=0,1\left(mol\right)\\ \Rightarrow n_{MgO}=\dfrac{18-0,1.10}{40}=0,2\left(mol\right)\\ n_{H_2SO_4\left(p.ứ\right)}=0,2+0,1=0,3\left(mol\right)< 1,12\left(mol\right)\\ \Rightarrow LoạiTH1\\ TH2:axit.dư\\ \Rightarrow\left\{{}\begin{matrix}40a+100b=18\\b=0,1\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\\ \Rightarrow\%m_{MgO}=\dfrac{0,2.40}{18}.100\approx44,444\%\Rightarrow\%m_{CaCO_3}\approx55,556\%\)
\(b,m_{ddB}=m_A+m_{ddH_2SO_4}-m_{CO_2}=18+500.1,12-0,1.44=573,6\left(g\right)\\ n_{H_2SO_4\left(dư\right)}=1,12-0,3=0,82\left(mol\right)\\ C\%_{ddH_2SO_4\left(dư\right)}=\dfrac{0,82.98}{573,6}.100\approx14,01\%\\ C\%_{ddCaCl_2}=\dfrac{0,1.111}{573,6}.100\approx1,935\%\\ C\%_{ddMgCl_2}=\dfrac{0,2.95}{573,6}.100\approx3,312\%\)
a)
\(m_{H_2SO_4}=\dfrac{300.19,6}{100}=58,8\left(g\right)\)
=> \(m_{dd.H_2SO_4.9,8\%}=\dfrac{58,8.100}{9,8}=600\left(g\right)\)
=> \(m_{H_2O\left(thêm\right)}=600-300=300\left(g\right)\)
b)
\(n_{HCl}=0,2.2=0,4\left(mol\right)\)
=> \(V_{dd.HCl.1,5M}=\dfrac{0,4}{1,5}=\dfrac{4}{15}\left(l\right)\)
=> \(V_{H_2O\left(thêm\right)}=\dfrac{4}{15}-0,2=\dfrac{1}{15}\left(l\right)=\dfrac{200}{3}\left(ml\right)\)
=> \(m_{H_2O\left(thêm\right)}=\dfrac{200}{3}.1=\dfrac{200}{3}\left(g\right)\)