Khử 8g Copper (II) oxide bằng khí hidrogen, vt pt và tính khối lượng kim loại thu được
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a. \(n_{Cu}=\dfrac{28.8}{64}=0,45\left(mol\right)\)
PTHH : CuO + H2 -> Cu + H2O
0,45 0,45 0,45 0,45
\(V_{H_2}=0,45.22,4=10,08\left(l\right)\)
b. \(m_{Cu}=0,45.64=28,8\left(g\right)\)
ncu = 28,8/64 = 0,45 mol
CuO + H2 -> Cu + H2O
1 : 1 : 1 : 1
0,45mol
a) nH2 = (0,45.1) : 1 = 0,45 mol
VH2 = 0,45 . 22,4 = 10,08 ( l )
b) mCu = 0,45 . 64 = 28,8 ( g)

nCu = 8: 80=0,1(mol)
a) PTHH : CuO + H2 -t--> Cu +H2O
0,1-> 0,1------>0,1(mol)
mCu = 0,1.64=6,4(g)
VH2 = 0,1.22,4=2,24(l)

Hiện tượng : kẽm bị tan dần , có khí không màu thoát ra .
Zn + 2HCl ---> ZnCl2 + H2
0,1 0,2 0,1 0,1
nZn = 6,5 / 65 = 0,1 ( mol )
V H2 = \(\dfrac{n.R.t}{p}=\dfrac{0,1.0,082.\left(273+25\right)}{1}=2,4436\left(l\right)\)
H2 + CuO ---> Cu + H2O
0,1 0,1
=> mCu = 0,1 . 64 = 6,4 (g)

nMg = 6/24 = 0,25 (mol)
PTHH: Mg + 2HCl -> MgCl2 + H2
nH2 = 0,25 (mol(
VH2 = 0,25 . 24,79 = 6,1975 (l)
CuO + H2 -> (t°) Cu + H2O
nCu = 0,25 (mol)
mCu = 0,25 . 64 = 16 (g)

\(H_2+CuO\rightarrow\left(t^o\right)Cu+H_2O\)
0,2 0,2 0,2 0,2
\(b,n_{Cu}=\dfrac{12,8}{64}=0,2\left(mol\right)\)
\(m_{CuO}=0,2.80=16\left(g\right)\)
\(V_{H_2}=0,2.24,79=4,958\left(l\right)\)
\(m_{H_2O}=0,2.18=3,6\left(g\right)\)
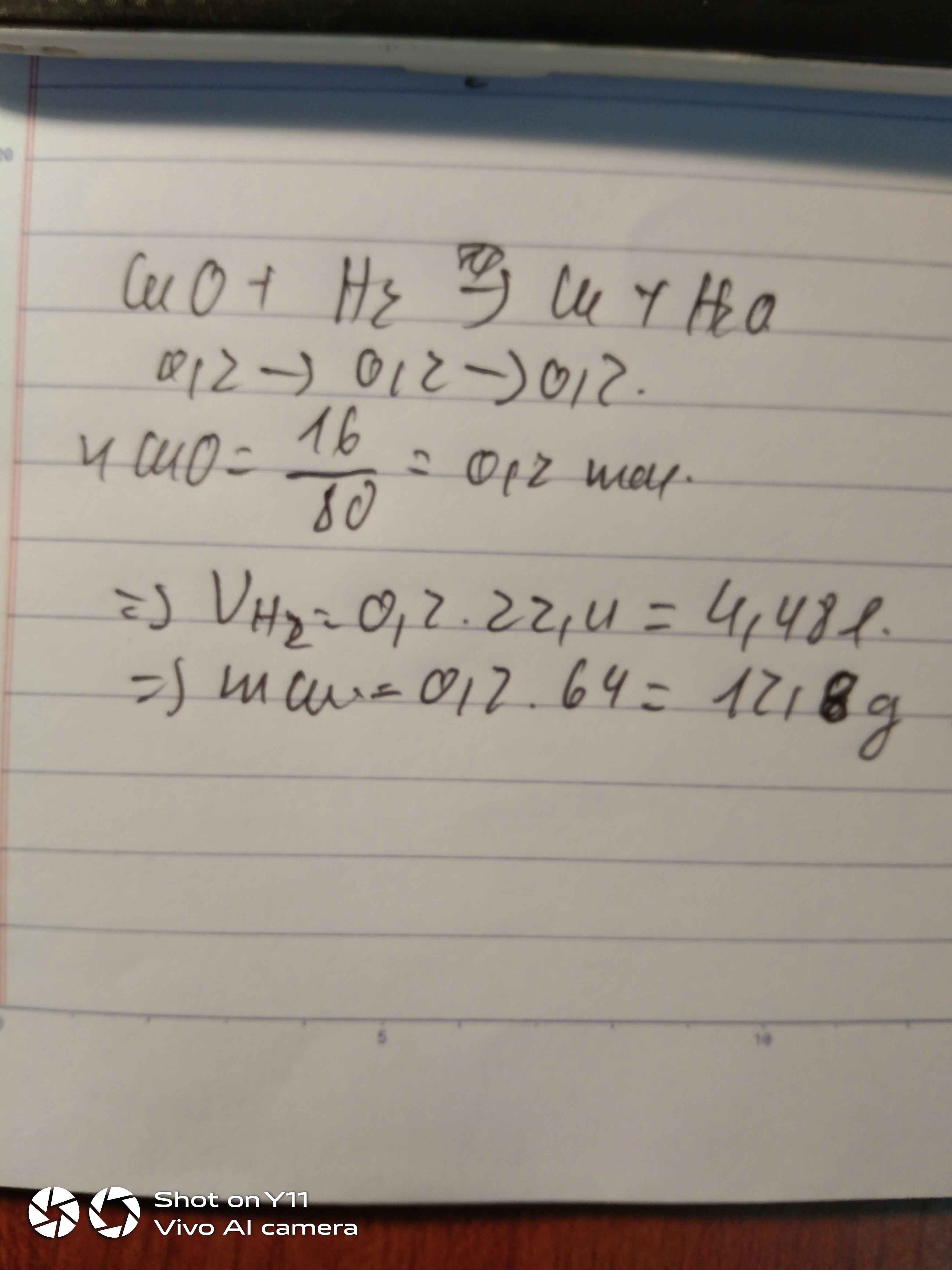
b ơi làm chi tiết giúp mình vs nha