Hoà tan 21,44g hỗn hợp X gồm MgO, CaO, Mg, Ca vào dung dịch HCl vừa đủ thu được 6,496 lít khí (đktc)và dung dịch Y trong đó có 24,7g MgCl2 và x(g) CaCl2. tính x
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


n H2 = 0,29 mol
n MgCl2= 0,26 mol
Các phương trình phản ứng ( gọi a,b,c,d lần lượt là số mol của ...)
MgO + 2HCl \(\rightarrow\) MgCl2 +H2O (1)
a a
Mg + 2HCl \(\rightarrow\) MgCl2 + H2 ( 2)
b b b
CaO + H2O \(\rightarrow\) Ca(OH)2 (3)
c c
Ca + 2H2O \(\rightarrow\) Ca(OH)2 + H2 (4)
d d d
Ca(OH)2 + 2HCl \(\rightarrow\) CaCl2 + 2H2O (5)
c+d c+d (cái này dựa vào pt (3) và (4) )
Theo đề ra ta có:
40a + 24b + 56c + 40d = 21,44 (I)
b + d = 0,29 (II)
a + b = 0,26 (III)
c + d = n CaCl2 (IV)
Biến đổi pt (I):
40a + 40b - 16b - 16d + 56d + 56c = 21,44
\(\Rightarrow\) 40(a+b) - 16(b+d) + 56(d+c) = 21,44 (V)
Thay (II) và (III) vào pt (V) ta có:
10,4 - 4,64 + 56(c+d) = 21,44
\(\Rightarrow\) 56(c+d) = 15,68 \(\Rightarrow\) c+d=0,28 = n CaCl2
\(\Rightarrow\) m CaCl2= 0,28 \(\times\) 111= 31,08 (g)
Vậy x = 31,08g

Giải thích:
nH2 = 0,145 mol
nMgCl2 = 0,13 mol
Quy đổi X thành: Mg (0,13 mol), Ca (x mol); O (y mol)
+ mX = 0,13.24 + 40x + 16y = 20,72
+ BT e: 2nMg + 2nCa = 2nH2 + 2nO => 0,13.2 + 2x = 0,145.2 + 2y
Giải hệ được x = 0,14; y = 0,125
mCaCl2 = 0,14.111 = 15,54 gam
Đáp án B

Đáp án : B
nH2 = nKL = 0,145 mol
Nếu cho X phản ứng với oxi dư tạo hỗn hợp D thì nO2 = 0,0725 mol
Xét hỗn hợp D :
=> moxit= 10,72 + 0,0725.32 = 13,04g
nMgO = nMgCl2 = 0,13 mol => nCaO = 0,14 mol = nCaCl2
=> m = 15,54g

Chọn D
nH2 = 0,145 mol
nMgCl2 = 12,35/95 = 0,13 mol
Quy dổi hỗn hợp ban đầu thành: Mg (0,13 mol), Ca (x mol), O (y mol).
+ Ta có: 0,13.24 + 40x + 16y = 10,72 (1)
+ BT e: 2nMg + 2nCa = 2nO + 2nH2
0,13.2 + 2x = 2y + 0,145.2 (2)
Giải (1) và (2) => x = 0,14; y = 0,125
mCaCl2 = 0,14.111 = 15,54 gam

Đáp án D
nH2 = 0,145 mol
nMgCl2 = 12,35/95 = 0,13 mol
Quy dổi hỗn hợp ban đầu thành:
Mg (0,13 mol), Ca (x mol), O (y mol).
+ Ta có: 0,13.24 + 40x + 16y = 10,72 (1)
+ BT e: 2nMg + 2nCa = 2nO + 2nH2
0,13.2 + 2x = 2y + 0,145.2 (2)
Giải (1) và (2)
=> x = 0,14; y = 0,125
mCaCl2 = 0,14.111 = 15,54 gam

Đáp án : B
Gọi số mol của Mg: x mol; Ca: y mol; O: z mol
Ta có: 24x+40y+16z=10,72
Bảo toàn e: 2x + 2y = 2z+2 . 0,145
x= nMgCl2=0,13
=> y =0,14 và z=0,125
=> m=0,14(40+71)=15,54 gam

Giải thích:
nH2 = 0,145 mol
nMgCl2 = 12,35/95 = 0,13 mol
Quy dổi hỗn hợp ban đầu thành: Mg (0,13 mol), Ca (x mol), O (y mol).
+ Ta có: 0,13.24 + 40x + 16y = 10,72 (1)
+ BT e: 2nMg + 2nCa = 2nO + 2nH2
0,13.2 + 2x = 2y + 0,145.2 (2)
Giải (1) và (2) => x = 0,14; y = 0,125
mCaCl2 = 0,14.111 = 15,54 gam
Đáp án D
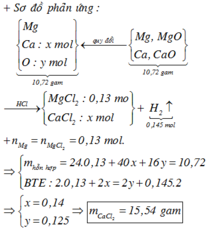
Quy đổi X thành \(\left\{{}\begin{matrix}Mg:a\left(mol\right)\\Ca:b\left(mol\right)\\O:c\left(mol\right)\end{matrix}\right.\)
Bảo toàn Mg: \(n_{Mg}=n_{MgCl_2}=\dfrac{24,7}{95}=0,26\left(mol\right)\)
Có: 24a + 40b + 16c = 21,44
=> 40b + 16c = 21,44 - 24.0,26 = 15,2 (1)
\(n_{H_2}=\dfrac{6,496}{22,4}=0,29\left(mol\right)\)
Mg0 - 2e --> Mg+2
0,26->0,52
Ca0 - 2e --> Ca+2
b--->2b
O0 + 2e --> O-2
c--->2c
2H+ + 2e --> H20
0,58<--0,29
Bảo toàn e: 0,52 + 2b = 2c + 0,58
=> 2b - 2c = 0,06 (2)
(1)(2) => a = 0,28; b = 0,25
=> \(n_{CaCl_2}=n_{Ca}=0,28\left(mol\right)\)
=> \(m_{CaCl_2}=0,28.111=31,08\left(g\right)\)