đốt cháy 4g bột than (chứa C và tạp chất rắn trơ ko cháy ) thu đc 6,72 lít khí CO2 ở đktc.tính độ tinh khiết của than
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Câu 1:
\(n_{CO_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: C + O2 --to--> CO2
0,15<-----------0,15
=> \(\%C=\dfrac{0,15.12}{2}.100\%=90\%\)
Câu 2:
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
0,2<-------------------0,3
=> mAl = 0,2.27 = 5,4 (g)
Câu 1.
\(n_{CO_2}=\dfrac{3,36}{22,4}=0,15mol\)
\(C+O_2\underrightarrow{t^o}CO_2\)
0,15 0,15
\(m_C=0,15\cdot12=1,8g\)
\(\%C=\dfrac{1,8}{2}\cdot100\%=90\%\)
Câu 2.
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3mol\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
0,2 0,3
\(m_{Al}=0,2\cdot27=5,4g\)

nKNO3 = 0.2 (mol)
2KNO3 -to-> 2KNO2 + O2
0.2__________0.2____0.1
mKNO2 = 0.2*85=17(g)
C + O2 -to-> CO2
x___x
S + O2 -to-> SO2
y___y
x + y = 0.1 (1)
Mặt khác :
+) 32y/m * 100% = 4%
=> 32y = 0.04m (2)
+) 12x/m = 0.92
=> 12x = 0.92m (3)
(1) , (2) , (3) :
x = 0.1
y = 0.002
m = 1.3
VCO2 + VSO2 = ( 0.1 + 0.002) * 22.4 = 2.2848 (l)

ĐÁP ÁN D
M = 15,75; nX = 48 kmol;
C + H2O -> CO + H2 C + 2H2O -> CO2 + 2H2
x--------------x------x y----------------y------2y kmol
Hỗn hợp X gồm x mol CO ; (x + 2y) mol H2 ; y mol CO2
Ta có : nX = 2x + 3y = 48; mX = 30x + 48y =756;
=> x = 6 ; y = 12;
=> m =18.12/(0,96.0,96) = 234,375 kg

X gồm O2 dư và CO2
CO2+ Ca(OH)2 -> CaCO3+ H2O
nCaCO3= nCO2= 0,08 mol
nX= 0,1 mol
=> nO2 dư= 0,02 mol
C+ O2 ⟶ CO2
=> nC= nO2 phản ứng= nCO2= 0,08 mol
Tổng nO2= 0,08+0,02= 0,1 mol
=> V= 2,24l
mC= 0,08.12= 0,96g
Than chứa 96% C nên lượng than đem đốt là 0,96:96%= 1g
Pt thứ 2 có nhiệt độ nha bn:)

Đổi: 24kg = 24000g
24kg than đá có chứa 0,5% tạp chất lưu huỳnh và 1,5% tạp chất khác không cháy được

⇒ nS = 120 / 32 = 3,75 mol
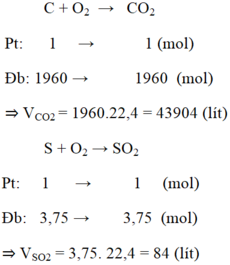

PT: \(C+O_2\underrightarrow{t^o}CO_2\) (1)
\(S+O_2\underrightarrow{t^o}SO_2\) (2)
Ta có: mS = 24.0,5% = 0,12 (kg) = 120 (g) ⇒ nS = 120/32 = 3,75 (mol)
Theo PT (2): \(n_{SO_2}=n_S=3,75\left(mol\right)\)
\(\Rightarrow V_{SO_2}=3,75.22,4=84\left(l\right)\)
Ta có: mC = 24 - 0,12 - 24.1,5% = 23,52 (kg) = 23520 (g)
\(\Rightarrow n_C=\dfrac{23520}{12}=1960\left(mol\right)\)
Theo PT (1): \(n_{CO_2}=n_C=1960\left(mol\right)\)
\(\Rightarrow V_{CO_2}=1960.22,4=43904\left(l\right)\)
Sửa: mC = 23,52 (kg) = 23420 (g)
⇒ \(n_C=\dfrac{23520}{12}=1960\left(mol\right)\)
Theo PT (1): \(n_{CO_2}=n_C=1960\left(mol\right)\)
\(\Rightarrow V_{CO_2}=1960.22,4=43904\left(l\right)\)
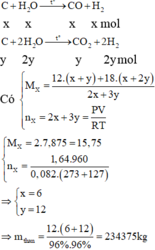
\(PTHH:C+O_2\underrightarrow{t^o}CO_2\)
\(n_{CO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Từ PTHH ta có
Đốt 1 mol C thì sinh ra 1 mol CO2
=> Đốt 0,3 mol C thì sinh ra 0,3 mol CO2
\(\Rightarrow m_C=0,3.12=3,6\left(g\right)\)
\(\Rightarrow\%C=\dfrac{3,6}{4}=90\%\)
Vậy độ tinh khiết của than là 90%