Một bình điện phân dùng để mạ bạc, có dòng điện 2 A chạy qua. Giả sử dòng điện này chỉ do ion Ag+ tạo ra. Tính số nguyên tử Ag bám vào cathode trong 20 phút. L
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Theo định luật I của Fa-ra-đây về điện phân, khối lượng bạc tới bám vào catôt tính bằng :
m = kIt
Từ đó suy ra dòng điện chạy qua bình điện phân phải có cường độ :
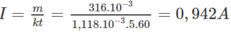
là chưa đúng và kết quả đo của ampe kế có sai số tỉ đối bằng :
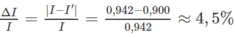

\(m=\dfrac{I.A.t}{F.n}=\dfrac{2.108.3.60}{96500.1}\approx0,4\left(kg\right)\)
\(m=D.V=D.S.h\Rightarrow h=\dfrac{m}{D.S}\approx0,056\left(m\right)\)

Lời giải:
Ta có khối lượng bạc bám ở cực âm: m = 1 F . A n I t → I = m F n A t = 27.96500.1 108.60.60 = 6 , 7 A
Đáp án cần chọn là: A

Đáp án A. Áp công thức của 2 định luật Faraday suy ra I = m n F A t = 27 . 1 . 96500 108 . 3600 = 6 , 7 A
