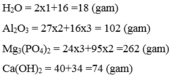Tính khối lượng của các chất sau:
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Câu 1 :
Trong $P_2O_5 : \%O = \dfrac{16.5}{31.2 + 16.5}.100\% = 56,34\%$
Trong $CaO : \%O = \dfrac{16}{40+16} .100\% = 28,57\%$
Trong $CO : \%O = \dfrac{16}{12 + 16}.100\% = 57,14\%$
Trong $Na_2O : \%O = \dfrac{16}{23.2 + 16}.100\% = 25,81\%$
Câu 2:
nH2=0,15(mol)
nFe2O3=0,1(mol)
PTHH: 3 H2 + Fe2O3 -to-> 2 Fe + 3 H2O
Ta có: 0,15/3 < 0,1/1
=> Fe2O3 dư, H2 hết, tính theo nFe2O3
nFe=2/3. nH2= 2/3. 0,15=0,1(mol) -> mFe=0,1.56=5,6(g)
nFe2O3(dư)= 0,1 - 1/3 . 0,15=0,05(g) -> mFe2O3=0,05.160=8(g)

`@` `\text {MgO}`
\(\text{PTK = 24 + 16 = 40 < amu>}\)
\(\%\text{O}=\dfrac{16\cdot100}{40}=40\%\)
Vậy, khối lượng `%` của `\text {O}` trong `\text {MgO}` là `40%`
`@` `\text {Fe}_2 \text {O}_3`
\(\text{PTK = }56\cdot2+16\cdot3=160\text{ }< \text{amu}\text{ }>\)
\(\%\text{Fe}=\dfrac{56\cdot2\cdot100}{160}=70\%\)
Vậy, khối lượng `%` của `\text {Fe}` trong `\text {Fe}_2 \text {O}_3` là `70%`

Vì dA/không khí = 2,07 ⇒ MA = 2,07.29 = 60
(vì Mkhông khí = 29)

\(n_{NaOH}=\dfrac{200.5\%}{100\%.40}=0,25(mol)\\ n_{HCl}=\dfrac{36,5.20\%}{100\%.36,5}=0,2(mol)\\ a,NaOH+HCl\to NaCl+H_2O\)
Vì \(\dfrac{n_{NaOH}}{1}>\dfrac{n_{HCl}}{1}\) nên \(NaOH\) dư
\(b,n_{NaOH(dư)}=0,25-0,2=0,05(mol);n_{NaCl}=0,2(mol)\\ \Rightarrow m_{\text{dd sau p/ứ}}=0,2.58,5+0,05.40=13,7(g)\\ c,m_{NaCl}=0,2.58,5=11,7(g)\\ d,n_{H_2}=0,2(mol)\\ \Rightarrow \begin{cases} C\%_{NaOH}=\dfrac{0,05.40}{36,5+200-0,2.2}.100\%=0,85\%\\ C\%_{NaCl}=\dfrac{11,7}{36,5+200-0,2.2}.100\%=4,96\% \end{cases}\)

\(\%_{N\left(\left(NH_2\right)_2CO\right)}=\dfrac{14.2}{\left(14+2\right).2+12+16}.100\%=46,67\%\\ \%_{N\left(NH_4NO_3\right)}=\dfrac{14.2}{14.2+4+16.3}.100\%=35\%\\ \%_{N\left(NH_4Cl\right)}=\dfrac{14}{14+4+35,5}.100\%=26,17\%\\ \%_{N\left(\left(NH_4\right)H_2PO_4\right)}=\dfrac{14}{14+4+2+31+16.4}.100\%=12,17\%\)
Vậy \((NH_2)_2CO\) có hàm lượng \(N\) cao nhất
M(NH2)2CO=60g/mol
\(\Leftrightarrow\) %N[(NH2)2CO]=\(\dfrac{14.2.100}{60}\)=47%
M NH4NO3=80g/mol
\(\Leftrightarrow\) %N(NH4NO3)=\(\dfrac{14.100}{80}\)= 18%
M NH4Cl=53,5g/mol
\(\Leftrightarrow\) %N(NH4Cl)=\(\dfrac{14.100}{53.5}\)=26%
M NH4H2PO4 = 115g/mol
\(\Leftrightarrow\) %N(NH4H2PO4)=\(\dfrac{14.100}{115}\)=12%
vậy hàm lượng N trong hợp chất (NH2)2CO lớn nhất

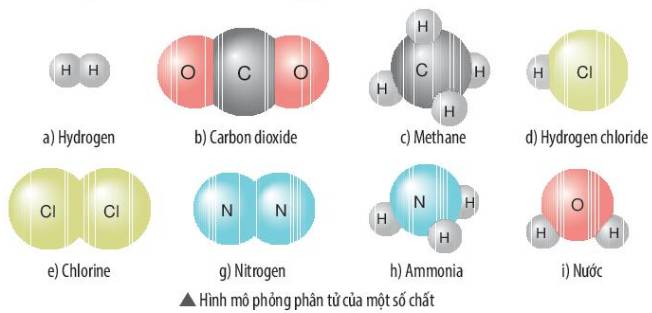
a) Hydrogen là đơn chất vì có cấu tạo từ một nguyên tố H.
Khối lượng phân tử Hydrogen: \(M_{H_2}=1
.
2=2\left(amu\right)\)
b) Carbon dioxide là hợp chất vì có cấu tạo từ 2 nguyên tố C và O.
Khối lượng phân từ Carbon dioxide: \(M_{CO_2}=12+16
.
2=44\left(amu\right)\)
c) Methane là hợp chất vì có cấu tạo từ 2 nguyên tố C và H.
Khối lượng phân tử Methane: \(M_{CH_4}=12+1
.
4=16\left(amu\right)\)
d) Hydrogen chloride là hợp chất vì có cấu tạo từ 2 nguyên tố H và Cl.
Khối lượng phân tử Hydrogen chloride: \(M_{HCl}=1+35,5=36,5\left(amu\right)\)
e) Chlorine là đơn chất vì có cấu tạo từ 1 nguyên tố là Cl.
Khối lượng phân tử Chlorine: \(M_{Cl_2}=35,5
.
2=71\left(amu\right)\)
g) Nitrogen là đơn chất vì có cấu tạo từ 1 nguyên tố N.
Khối lượng phân tử Nitrogen: \(M_{N_2}=14
.
2=28\left(amu\right)\)
h) Ammonia là hợp chất vì có cấu tạo từ 2 nguyên tố N và H.
Khối lượng phân tử Ammonia: \(M_{NH_3}=14+1
.
3=17\left(amu\right)\)
i) Nước là hợp chất vì có cấu tạo từ 2 nguyên tố H và O.
Khối lượng phân tử Nước: \(M_{H_2O}=1
.
2+16=18\left(amu\right)\)
đơn chất: hydro, clo, nitơ
hợp chất: carbon dioxide, methane, hydrogen chloride, ammonia, nước
Nguyên tử khối:
hydrogen: 2
clo: 35,5*2=71
nitơ: 28
Carbon dioxide: 44
Metan: 16
Hydrogen chloride: 36,5
Ammoniac: 17
Nước: 18

Trong CO2 và K2SO4 không có N mà bạn nhỉ?
HNO2: \(\%m_N=\dfrac{14}{1+14+16.2}.100\%\approx29,79\%\)
NaNO3: \(\%m_N=\dfrac{14}{23+14+16.3}.100\%\approx16,47\%\)