Hòa tan hoàn toàn 6,12 gam Al2O3 trong 200ml dung dịch HCl 2M thu được dung dịch A. Tính thể tích dung dịch NaOH 2M cần thêm vào dung dịch A để thu được 7,8 gam kết tủa.
Giúp mình vs mình cần gấp. Thanks mn <3
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án A
Câu này rất đơn giản dữ kiện 0,54 gam Al không cần thiết.Kết tủa lớn nhất khi Na trong NaOH chạy vào NaCl và Na2SO4
Ta có

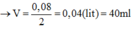

Giải thích:
X gồm HCl dư (x mol) và AlCl3 (y mol)
=> x = 0,1 mol
+ Tại nNaOH = 0,25 mol: nNaOH = nHCl + 3nAl(OH)3 => nAl(OH)3 = (0,25-0,1)/3 = 0,05 mol
+ Tại nNaOH = 0,45 mol: nNaOH = nHCl + 4nAl3+ - nAl(OH)3 => 0,45 = 0,1 + 4y – 0,05 => y = 0,1 mol
BT “Cl” => nHCl = 3nAlCl3 + nHCl dư => nHCl = 0,1 + 3.0,1 = 0,4 mol
=> a = 0,4/0,2 = 2M
Đáp án A

Đáp án A
Khi cho hỗn họp gồm Na2O và A12O3 có phản ứng:
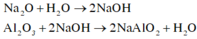
Vì sau một thời gian cho HCl vào dung dịch A mới xuất hiện kết tủa nên A gồm NaA1O2 và NaOH dư
Thứ tự các phản ứng xảy ra:
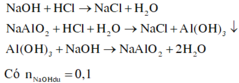
Vì khi cho 200ml hoặc 600ml dung dịch HCl 1M đều thu được a gam kết tủa nên khi cho 200ml dung dịch HCl thì chưa có sự hòa tan kết tủa và khi cho 600ml dung dịch HCl thì đã có sự hòa tan kết tủa.
Do đó:
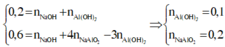
Áp dụng định luật bảo toàn nguyên tố cho Al và Na có
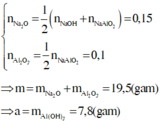

Hòa tan 0,02 mol Al2O3 hết 0,12 mol HCl
Dung dịch thu được có 0,04 mol AlCl3 và 0,02 mol HCl dư
HCl + NaOH → NaCl + H2O
AlCl3 + 3NaOH à 3NaCl + Al(OH)3
Trug hòa hết 0,02 mol NaOH. Tạo kết tủa cực đại hết 0,12 mol NaOH được 0,04 mol Al(OH)3
Để chỉ còn 0,01 mol kết tủa cần hòa tan 0,04 - 0,01 = 0,03 mol kết tủa => cần thêm 0,03 mol NaOH Tổng số mol NaOH đã đem dùng là
0,02 + 0,12 + 0,03 = 0,17 mol
=> Đáp án A

nNaOH ban đầu = 0,4 mol
Al + NaOH ⟶ NaAlO2 + 3/2H2
0,1 0,1 0,15
![]()
Al2O3 + 2NaOH⟶2NaAlO2 + H2O
a 2a
(dư 0,3-2a)
⟶ m = 2,7 + 102a.
Lập hệ phương trình →a = 0.05 → m = 7,8
Đáp án B
PTHH: \(Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\) (1)
\(HCl+NaOH\rightarrow NaCl+H_2O\) (2)
\(AlCl_3+3NaOH\rightarrow3NaCl+Al\left(OH\right)_3\downarrow\) (3)
Ta có: \(\left\{{}\begin{matrix}n_{Al_2O_3}=\dfrac{6,12}{102}=0,06\left(mol\right)\\\Sigma n_{HCl}=0,2\cdot2=0,4\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,06}{1}< \dfrac{0,4}{6}\) \(\Rightarrow\) HCl còn dư, Al2O3 p/ứ hết
Vì bazơ mạnh sẽ p/ứ với axit mạnh trước nên sẽ xảy ra p/ứ (2) và (3)
Lại có: \(n_{Al\left(OH\right)_3}=\dfrac{7,8}{78}=0,1\left(mol\right)=n_{AlCl_3\left(3\right)}\)
Theo PTHH (1): \(n_{AlCl_3\left(1\right)}=0,12\left(mol\right)\)
\(\Rightarrow\) AlCl3 còn dư nên tính theo Al(OH)3 \(\Rightarrow n_{NaOH\left(3\right)}=0,3\left(mol\right)\)
Mặt khác: \(n_{HCl\left(dư\right)}=n_{HCl\left(2\right)}=0,04\left(mol\right)=n_{NaOH\left(2\right)}\)
\(\Rightarrow\Sigma n_{NaOH}=0,34\left(mol\right)\) \(\Rightarrow V_{NaOH}=\dfrac{0,34}{2}=0,17\left(l\right)=170\left(ml\right)\)
Bạn tham khảo xem có đúng hay không, mình ko chắc lắm