Hòa tan 34 g hỗn hợp G gồm MgO và Zn vào dung dịch HCl dư thu được 73,4 g hỗn hợp muối G'.Tính % khối lượng từng chất trong G.
GIẢI RÕ RÀNG RA DÙM MÌNH MÌNH CẦN RẤT GẤP TỐI NAY LÚC 10H GIÚP DÙM MÌNH
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

PTHH: MgO + 2 HCl -> MgCl2 + H2
x__________2x_______x______x(mol)
Zn + 2 HCl -> ZnCl2 + H2
y____2y_____y_____y(mol)
Ta có:
\(\left\{{}\begin{matrix}40x+65y=34\\95x+136y=73,4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,4\end{matrix}\right.\)
mMgO= 0,2.40=8(g)
=> %mMgO= \(\frac{8}{34}.100\approx23,529\%\)
=> %mZn \(\approx100\%-23,529\%\approx76,471\%\)

Gọi số mol của MgO và Zn là a và b
=> 40a + 65b = 34
PTHH: MgO + 2HCl --> MgCl2 + H2O
______a------------------->a
Zn + 2HCl --> ZnCl2 + H2
b---------------->b
=> 95a + 136b = 73,4
=> a = 0,2; b = 0,4
=> \(\left\{{}\begin{matrix}\%MgO=\dfrac{0,2.40}{34}.100\%=23,529\%\\\%Zn=\dfrac{0,4.65}{34}.100\%=76,471\%\end{matrix}\right.\)

Gọi \(\left\{{}\begin{matrix}n_{CuO}=x\\n_{MgO}=y\end{matrix}\right.\)
\(CuO+2HCl\rightarrow CuCl_2+H_2O\)
x x ( mol )
\(MgO+2HCl\rightarrow MgCl_2+H_2O\)
y y ( mol )
Ta có:
\(\left\{{}\begin{matrix}80x+40y=16\\135x+95y=32,5\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
\(\Rightarrow m_{CuO}=0,1.80=8g\)
\(\Rightarrow m_{MgO}=0,2.40=8g\)
\(\%m_{CuO}=\dfrac{8}{16}.100=50\%\)
\(\%m_{MgO}=\dfrac{8}{16}.100=50\%\)
\(m_{CuCl_2}=0,1.135=13,5g\)
\(m_{MgCl_2}=0,2.95=19g\)

Chọn A
Bảo toàn khối lượng : mKL + mO = moxit => nO = 0,26 mol
Khi oxit phản ứng với HCl thì cũng tương tự như 1 mol O bị thay thế bởi 2 mol Cl-
=> nCl = 2nO = 0,52 mol
=> mKL + mCl = mmuối => m + 0,52.35,5 = 3m + 1,82
=> m = 8,32g
, mkết tủa = 9m + 4,06 = 78,94g
,nAgCl = nCl = 0,52 mol => Giả sử có Ag => nAg = 0,04 mol
Fe2+ + Ag+ -> Fe3+ + Ag
=> nFe2+ = nAg = 0,04 mol => nFeO(X) = 0,04
Vậy trong 3,75m (g) hỗn hợp X ( 31,2g) sẽ có nFeO = 0,04.31,2/(8,32 + 4,16) = 0,1
Khi phản ứng với HNO3 thì FeO -> Fe(NO3)3 ( Fe2+ -1e -> Fe3+)
Xét 3,75m gam X : Ta thấy nCl(muối) = ne trao đổi (1) = 1,3 mol
Khi phản ứng với HNO3 thì ne trao đổi (2) = ne trao đổi (1) + nFeO = nNO3 muối = 1,4 mol
=> m’ = mKL + mNO3 = 8,32.2,5 + 1,4.62 = 107,6g
( Nếu xét trường hợp không tạo NH4NO3)

Áp dụng tăng giảm khối lượng, ta thấy 1 nguyên tử O được thay thế bởi 2 nguyên tử Cl.
ZnO, PbO, NiO → Z n C l 2 , P b C l 2 , N i C l 2
⇒ Từ 1 mol oxit ban đầu khối lượng muối sau phản ứng tăng là:
m↑= m 2 C l - m O = 2.35,5 - 16 = 55g
m h h b a n d a u = m F e 3 O 4 + m C u p ư = , 12 . 232 + 0 , 12 . 64 + 8 , 32 = 43 , 84 g
Theo bài ra, ta có:
m↑ = m m u o i - m h h o x i t = (b +55) - b = 55g
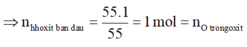
⇒mX = m h h o x i t b a n d a u - m O =b-16 = a
⇒ Chọn A.

\(n_{H_2SO_4}=\dfrac{19,6\%.500.1,12}{98}=1,12\left(mol\right)\\n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ MgO+H_2SO_4 \rightarrow MgSO_4+H_2O\\ CaCO_3+H_2SO_4\rightarrow CaSO_4+CO_2+H_2O\\ TH1:axit.hết\\ n_{CO_2}=n_{CaCO_3}=0,1\left(mol\right)\\ \Rightarrow n_{MgO}=\dfrac{18-0,1.10}{40}=0,2\left(mol\right)\\ n_{H_2SO_4\left(p.ứ\right)}=0,2+0,1=0,3\left(mol\right)< 1,12\left(mol\right)\\ \Rightarrow LoạiTH1\\ TH2:axit.dư\\ \Rightarrow\left\{{}\begin{matrix}40a+100b=18\\b=0,1\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\\ \Rightarrow\%m_{MgO}=\dfrac{0,2.40}{18}.100\approx44,444\%\Rightarrow\%m_{CaCO_3}\approx55,556\%\)
\(b,m_{ddB}=m_A+m_{ddH_2SO_4}-m_{CO_2}=18+500.1,12-0,1.44=573,6\left(g\right)\\ n_{H_2SO_4\left(dư\right)}=1,12-0,3=0,82\left(mol\right)\\ C\%_{ddH_2SO_4\left(dư\right)}=\dfrac{0,82.98}{573,6}.100\approx14,01\%\\ C\%_{ddCaCl_2}=\dfrac{0,1.111}{573,6}.100\approx1,935\%\\ C\%_{ddMgCl_2}=\dfrac{0,2.95}{573,6}.100\approx3,312\%\)

Đáp án D
Al2O3 và MgO không bị khử bởi CO
Y: Al2O3; MgO; Fe; Cu
Y + NaOH: chỉ có Al2O3 phản ứng
G + Cu(NO3)2: chỉ có Fe phản ứng
=> F gồm: MgO; Cu

Đáp án D
Al2O3 và MgO không bị khử bởi CO
Y : Al2O3 ; MgO ; Fe ; Cu
Y + NaOH : chỉ có Al2O3 phản ứng
G + Cu(NO3)2 : chỉ có Fe phản ứng
=> F gồm : MgO ; Cu
Gọi : \(\left\{{}\begin{matrix}n_{MgO}=a\left(mol\right)\\n_{Zn}=b\left(mol\right)\end{matrix}\right.\)⇒ 40a + 65b = 34(1)
\(MgO + 2HCl \to MgCl_2 + H_2O\\ Zn + 2HCl \to ZnCl_2 + H_2O\)
Muối gồm :\(\left\{{}\begin{matrix}n_{MgCl_2}=a\left(mol\right)\\n_{ZnCl_2}=b\left(mol\right)\end{matrix}\right.\)
Suy ra : 95a + 136b = 73,4(2)
Từ (1)(2) suy ra a = 0,2 ; b = 0,4
Vậy :
\(\%m_{MgO} = \dfrac{0,2.40}{34} .100\% = 23,53\%\\ \%m_{Zn} = 100\% - 23,53\% = 76,47\%\)