Có ba mẫu hợp kim có cùng khối lượng: Al-Cu, Cu-Ag, Mg-Al. Dùng chất nào sau đây để có thể phân biệt ba mẫu hợp kim trên?
A. KOH.
B. HCl.
C. HNO3.
D. H2SO4.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
Hướng dẫn Trích mẩu thử cho mỗi lần thí nghiệm. Cho dung dịch H2SO4 lần lượt vào các mẩu thử.
- Hợp kim nào không có khí là Cu-Ag.
- Cho dung dịch NH3 vào dung dịch thu được trong hai trường hợp còn lại.
+ Trường hợp tạo kết tủa keo trắng và không tan trong NH3 dư => hợp kim là Cu-Al.
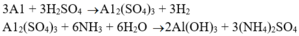
+ Trường hợp tạo kết tủa rồi tan trong NH3 dư => hợp kim ban đầu là Cu-Zn.


Đáp án D
Trích mẩu thử cho mỗi lần thí nghiệm. Cho dung dịch H2SO4 lần lượt vào các mẩu thử.
- Hợp kim nào không có khí là Cu-Ag.
- Cho dung dịch NH3 vào dung dịch thu được trong hai trường hợp còn lại.
+ Trường hợp tạo kết tủa keo trắng và không tan trong NH3 dư => hợp kim là Cu-Al.
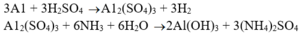
+ Trường hợp tạo kết tủa rồi tan trong NH3 dư => hợp kim ban đầu là Cu-Zn.
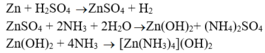

-Trích mẩu thử cho mỗi lần thí nghiệm.
-Cho dung dịch H2SO4 lần lượt vào các mẩu thử.
- >Hợp kim nào không có khí là Cu-Ag.
- Cho dung dịch NH3 vào dung dịch thu được trong hai trường hợp còn lại.
+ Trường hợp tạo kết tủa keo trắng và không tan trong NH3 dư => hợp kim là Cu-Al.
+ Trường hợp tạo kết tủa rồi tan trong NH3 dư => hợp kim ban đầu là Cu-Zn.

Đáp án D.
- Cho dd H2SO4 loãng lần vào các mẫu thử:
+ Mẫu có khí thoát ra có có kết tủa trắng là Ba
Ba + H2SO4 → BaSO4↓ + H2↑
+ Mẫu có khí thoát ra và dung dịch muối thu được có màu trắng xanh là Fe
Fe + H2SO4 → FeSO4 + H2↑
+ Mẫu không tan là Ag
+ 2 mẫu còn lại cùng có khí không màu thoát ra là Al và Mg
Mg + H2SO4 → MgSO4 + H2↑
2Al + 3H2SO4 → Al2(SO4)3 + 3H2↑
- Lấy một lượng dư kim loại Ba (đã nhận biết được ở trên) nhỏ vài giọt dd H2SO4 loãng đến sẽ xảy ra phản ứng
Ba + H2SO4 → BaSO4↓ + H2↑
Ba + 2H2O → Ba(OH)2 + H2↑
Lọc bỏ kết tủa BaSO4↓ ta thu được dd Ba(OH)2
- Cho Ba(OH)2 lần lượt vào 2 mẫu thử chưa nhận biết được là Mg và Al
+ Kim loại nào thấy khí thoát ra là Al
2Al + 2H2O + Ba(OH)2 → Ba(AlO2)2 + 2H2↑
+ Kim loại nào không có hiện tượng gì là Mg
⇒ Vậy sẽ nhận ra được cả 5 kim loại

D
- Hòa tan các mẫu hợp kim vào H2O dư:
+ Chất rắn không tan: Mg-Al, Mg-Ag (1)
+ Chất rắn tan 1 phần, có khí thoát ra: Mg-K
\(2K+2H_2O\rightarrow2KOH+H_2\)
- Lọc lấy dd thu được sau khi hòa tan Mg-K vào nước, cho 2 hợp kim ở (1) tác dụng với dd thu được:
+ Chất rắn không tan: Mg-Ag
+ Chất rắn tan 1 phần, có khí thoát ra: Mg-Al
\(2Al+2KOH+2H_2O\rightarrow2KAlO_2+3H_2\)
Dùng dung dịch HCl để phân biệt ba mẫu hợp kim trên:
Al-Cu
Cu-Ag
Mg-Al
Dung dịch HCl
Tan một phần
Không tan
Tan hoàn toàn
Phương trình phản ứng: