Hãy chọn nửa sơ đồ phản ứng ở cột II để ghép với nửa sơ đồ phản ứng II cột I cho phù hợp.
Cột I
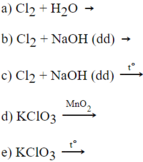
Cột II
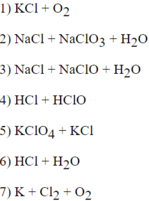
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.
Hãy chọn nửa sơ đồ phản ứng ở cột II để ghép với nửa sơ đồ phản ứng II cột I cho phù hợp.
Cột I
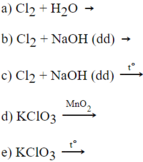
Cột II
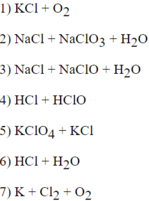


Chổ này H2 phải là 0.2 (g) nhé !
Áp dụng định luật bảo toàn khối lượng :
\(m_{Fe}+m_{HCl}=m_{FeCl_2}+m_{H_2}\)
\(m_{HCl}=12.7+0.2-5.6=7.3\left(g\right)\)
- Theo ĐLBTKL: \(m_{Fe}+m_{HCl}=m_{FeCl_2}+m_{H_2}\)
=> \(m_{HCl}=12,7+0,2-5,6=7,3\left(g\right)\)
Check lại đề chứ 0,1 mol Fe pư s ra đc 1 mol H2 :D

a) Theo đề bài, ta có:
nFe= \(\frac{m_{Fe}}{M_{Fe}}=\frac{28}{56}=0,5\left(mol\right)\)
PTHH: Fe + 2HCl -> FeCl2 + H2
Theo PTHH : 1:2:1:1 (mol)
Theo đề bài: 0,5:1:0,5:0,5 (mol)
b) Theo PTHH và đề bài, ta có:
\(n_{FeCl_2}=n_{Fe}\)= 0,5 (mol)
Khối lượng sắt clorua tạo thành:
\(m_{FeCl_2}=n_{FeCl_2}.M_{FeCl_2}=0,5.127=63,5\left(g\right)\)
c) nFe= \(\frac{m_{Fe}}{M_{Fe}}=\frac{14}{56}=0,25\left(mol\right)\)
Theo PTHH và đề bài, ta được:
nHCl= 2.nFe= 2.0,25=0,5 (mol)
Khối lượng HCl đã phản ứng:
mHCl=nHCl . MHCl= 0,5 . 36,5 = 18,25 (g)
a)
PTHH : Fe + 2HCl ---) FeCl2 + H2
b)
Số mol của Sắt là :
\(n_{Fe}=\frac{m_{Fe}}{M_{Fe}}=\frac{28}{56}=0,5\left(mol\right)\)
PTHH : Fe + 2HCl ---) FeCl2 + H2
Theo PTHH : 1 : 2 : 1 : 1 (mol)
Théo bài ra : 0,5--)1---------)0,5--------)0,5 (mol)
Khối lượng FeCl2 tạo thành là :
\(m_{FeCl_2}=n_{FeCl_2}\times M_{FeCl_2}=0,5\times\left(56+2\times\left(35,5\right)\right)=63,5\left(g\right)\)
Nếu phân nửa lượng sắt trên thành 14 g sắt thì số mol của sắt là :
\(n_{Fe}=\frac{m_{Fe}}{M_{Fe}}=\frac{14}{56}=0,25\left(mol\right)\)
mà Số mol của HCl gấp 2 lần số mol của sắt
Suy ra Nếu lấy phân nửa lượng sắt thì cần 0,5 mol HCl để phản ứng
Vậy khối lượng của HCl là :
\(m_{HCl}=n_{HCl}\times M_{HCl}=0,5\times\left(1+35,5\right)=18,25\left(g\right)\)
Chúc bạn học tốt =))![]()

Mỗi phản ứng xảy ra với 1 phân tử H 2 và 1 phân tử CuO, tạo ra 1 phân tử H 2 O và 1 nguyên tử Cu.
a-4; b-3; c-2; d-1; e-5