Cho m gam bột sắt vào 200 ml dung dịch HNO3 4M. Sau phản ứng hoàn toàn, thu được khí NO (sản phẩm khử duy nhất) và còn lại 1 gam bột sắt chưa tan. Giá trị của m là
A. 16,8
B. 17,8
C. 15,0
D. 12,2
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án B.
Sau phản ứng thu được chất rắn => thu được Fe2+
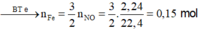
⇒ m = 0 , 15 . 56 + 2 , 4 = 10 , 8 gam

Đáp án B
→
B
T
e
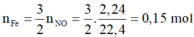
![]()
Sau phản ứng thu được chất rắn => thu được Fe2+

Đáp án A
- P1: hỗn hợp rắn X + HCl → H2 => chứng tỏ Fe dư, Cu2+ phản ứng hết.
Fe + 2HCl → FeCl2 + H2
=> nFe(1) = nH2 = 2,24: 22,4 = 0,1 mol
- P2: X + HNO3 → NO => Cả Fe và Cu đều phản ứng
Giả sử số mol ở phần 2 gấp k lần phần 1. Gọi số mol Cu phần 1 là a
Bảo toàn electron: 3nFe(2) + 2nCu(2) = 3nNO = 3.6,72: 22,4 = 0,9 mol
=> 3.0,1k + 2.ak = 0,9 (*)
Bảo toàn nguyên tố Cu: nCuSO4 = nCu(1) + nCu(2) => 0,2 = a + ak => a = 0 , 2 k + 1
Thay vào (*) =>0,3k + 2k. 0 , 2 k + 1 = 0,9
=> k = 2,097
- Vì Fe dư sau phản ứng nên: nFe pứ = nCuSO4 = 0,2 mol
=> nFe = nFe pứ + nFe(1) + nFe(2) = 0,3 + 0,1k = 0,5097 mol
=> mFe = 28,5432g (Gần nhất với giá trị 28,2g)

4H+ + NO3- +3e -> NO +2H2O
=>nNO=0,18
Dung dịch sau phản ứng gồm 0,48 mol Fe2+ ; x mol Cu2+, 0,3 mol NO3- ; 0,72 mol Na+ và 0,72 mol SO42-
Bảo toàn điện tích => x=0,03
Bảo toàn Cu : m+0,03.64=0,24.64 => m=13,44g
=> Đáp án D
Chọn B