Nung 27,2 gam hỗn hợp sắt (III) hidroxit và magie hidroxit đến khi phản ứng hoàn toàn thấy khối lượng chất rắn thu được giảm 7,2 gam so với khối lượng hidroxit ban đầu. Tính khối lượng chất rắn tạo thành và phần trăm khối lượng mỗi hidroxit.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


- PTHH: 2Al(OH)3\(\underrightarrow{t^0}\)Al2O3+3H2O
Zn(OH)2\(\underrightarrow{t^0}\)ZnO+H2O
- Khối lượng chất rắn giảm chính là khối lượng nước tạo thành
\(\rightarrow\)\(n_{H_2O}=\dfrac{m}{M}=\dfrac{1,98}{18}=0,11mol\)
- Gọi số mol Al(OH)3 là x và Zn(OH)2 là y ta có hệ phương trình:
\(\left\{{}\begin{matrix}78x+99y=6,66\\\dfrac{3x}{2}+y=0,11\end{matrix}\right.\)
- Giải ra x=0,06 và y=0,02
- Thành phần phần trăm khối lượng mỗi hidroxit là:
\(\%m_{Al\left(OH\right)_3}=\dfrac{0,06.78.100}{6,66}\simeq70,27\%\)
\(\%m_{Zn\left(OH\right)_2}=100\%-70,27\%=29,73\%\)


| CHÚ Ý |
| + Nhiệt phân (NH4)2CO3 sẽ cho ra NH3. Khí NH3 có thể khử CuO về Cu + Chất rắn Y không tan hoàn toàn trong axit H2SO4 loãng nên có phải chứa hỗn hợp CuO và Cu. |

Ta có: \(\left\{{}\begin{matrix}n_{MgO}=\dfrac{6}{40}=0,15\left(mol\right)\\n_{HCl}=0,05\cdot0,4=0,02\left(mol\right)\end{matrix}\right.\)
Bảo toàn nguyên tố: \(\left\{{}\begin{matrix}n_{Mg\left(OH\right)_2}=n_{MgO}=0,15\left(mol\right)\\n_{NaOH}=n_{NaCl}=n_{HCl}=0,02\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow a=m_{NaOH}+m_{Mg\left(OH\right)_2}=0,02\cdot40+0,15\cdot58=9,5\left(g\right)\)
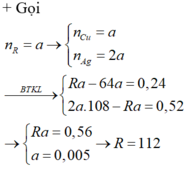
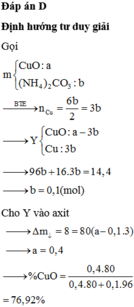

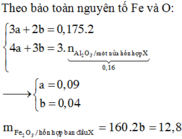
b = 0,1 bn nhé
mik đánh nhầm
Gọi số mol Fe(OH)3, Mg(OH)2 là a,b (mol)
PTHH: \(2Fe\left(OH\right)_3\underrightarrow{t^o}Fe_2O_3+3H2O\)
________a ------------> 0,5a____________(mol)
\(Mg\left(OH\right)_2\underrightarrow{t^o}MgO+H_2O\)
b-----------------> b_________(mol)
=> \(\left\{{}\begin{matrix}107a+58b=27,2\\160.0,5a+40b=27,2-7,2\end{matrix}\right.\) => \(\left\{{}\begin{matrix}a=0,2\left(mol\right)\\b=0,11\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}m_{Fe\left(OH\right)_3}=0,2.107=21,4\\m_{Mg\left(OH\right)_2}=0,1.58=5,8\left(g\right)\\m_{Fe_2O_3}=160.0,5.0,2=16g\\m_{MgO}=40.0,1=4\left(g\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}\%m_{Fe\left(OH\right)_3}=\frac{21,4}{27,2}.100\%=78,68\%\\\%m_{Mg\left(OH\right)_2}=\frac{5,8}{27,2}.100\%=21,32\%\end{matrix}\right.\)