Cho m gam chất A là hợp chất của natri tác dụng với HCl 10%, phản ứng xảy ra hoàn toàn thu được dung dịch B, không có chất khí hoặc kết tủa tạo ra. Trong dung dịch B nồng độ của HCl là 1460/227 % . Trung hòa lượng axit dư trong dung dịch B bằng dung dịch NaOH thu được dung dịch muối C, cô cạn dung dịch C thu được duy nhất muối NaCl khan có khối lượng 17,55 gam. Tính m ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Do Y tác dụng được với HCl nên Y chứa Fe dư ⇒ C u 2 + hết
Giả sử chỉ có Mg phản ứng ![]()
=> tăng giảm khối lượng ![]()
=> vô lý => Fe phản ứng
Bảo toàn khối lượng gốc kim loại:
24x + 56y = 9,2 + 0,13.64 - 12,48 => x = 0,07 mol; y = 0,06 mol
=> rắn gồm 0,07 mol MgO và 0,03 mol F e 2 O 3 => m = 7,6 (g)

Đáp án A
Do Y tác dụng được với HCl nên Y chứa Fe dư => C u 2 + hết
Giả sử chỉ có Mg phản ứng

Bảo toàn khối lượng gốc kim loại:
![]()
![]()
=> rắn gồm 0,07 mol MgO và 0,03 mol
![]()

Đáp án A
Do Y tác dụng được với HCl nên Y chứa Fe dư ⇒ C u 2 + hết
Giả sử chỉ có Mg phản ứng ![]()
=> tăng giảm khối lượng ![]()
=> vô lí => Fe phản ứng
Bảo toàn khối lượng gốc kim loại:
24x + 56y = 9,2 + 0,13.64 - 12,48 => x = 0,07 mol => m = 7,6(g)
=> rắn gồm 0,07 mol MgO và 0,03 F e 2 O 3 => m = 7,6 (g)

Chọn đáp án A.
« Trắc nghiệm: Y + HCl dư → 0,04 mol H2; khả năng cao nhất là do 0,04 mol Fe.
12,48 gam Y gồm 0,04 mol Fe + 0,13 mol Cu (từ dung dịch ra) + ? mol Cu ban đầu → ? = 0,03 mol.
Đơn giản lại quá trình:
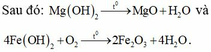
Ta có Z gồm 0,07 mol MgSO4 và 0,06 mol FeSO4 → Khi cho Z + NaOH thu được Mg(OH)2 và Fe(OH)2.
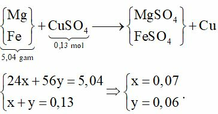
Suy ra m gam chất rắn gồm 0,07 mol MgO và 0,03 mol Fe2O3 → m=7,6 gam.
« Tự luận: cần lập luận chặt chẽ hơn chút. Đó là có thể Mg còn dư trong Y. Nhưng sẽ là dễ thấy ngay TH này không thỏa mãn. Thật vậy, khi đó Z chỉ chứa duy nhất 0,13 mol MgSO4.
→ BTKL phản ứng đầu có m=14,4 mâu thuẫn giả thiết.!

Đáp án A
Do Y tác dụng được với HCl nên Y chứa Fe dư => C u 2 + hết
Giả sử chỉ có Mg phản ứng
![]()
=> tăng giảm khối lượng
![]()
=>vô lí => phản ứng
Bảo toàn khối lượng gốc kim loại:
![]()
![]()
=> rắn gồm 0,07 mol MgO và 0,03 mol
![]()





Theo dữ kiện đề bài, ta xác định A có thể là \(Na_2O\) hoặc \(NaOH\)
\(TH_1:A:Na_2O\)
Gọi số mol Na2O là a(mol) và dd HCl pứ x(g) dd
\(n_{HCl}=\frac{x.10}{100.36,5}=\frac{x}{365}\left(mol\right)\)
\(PTHH:Na_2O+2HCl\rightarrow2NaCl+H_2O\)
(mol)________a___2a________2a__________
\(C\%_{HCl}=\frac{36,5.\left(\frac{x}{365}-2a\right)}{62a+x}.100=\frac{1460}{227}\left(A\right)\)
\(PTHH:NaOH+HCl\rightarrow NaCl+H_2O\)
(mol)______\(\left(\frac{x}{365}-2a\right)\)_____\(\left(\frac{x}{365}-2a\right)\)
Qua 2 pứ thì NaCl thu được là:
\(58,5\left(2a+\frac{x}{365}-2a\right)=17,55\Rightarrow x=109,5\left(g\right)\)
Thay x vừa tìm vào (A) và giải:
\(\Rightarrow a=0,05\left(mol\right)\Rightarrow m=62a=62.0,05=3,1\left(g\right)\)
\(TH_2:A:NaOH\)
Gọi số mol NaOH là a(mol) và dd HCl pứ x(g) dd
\(n_{HCl}=\frac{x}{365}\left(mol\right)\)
\(PTHH:NaOH+HCl\rightarrow NaCl+H_2O\)
(mol)______a_______a_______a_____________
\(C\%_{HCl}=\frac{36,5.\left(\frac{x}{365}-a\right)}{40a+x}.100=\frac{1460}{227}\left(A\right)\)
\(PTHH:NaOH+HCl\rightarrow NaCl+H_2O\)
(mol)__________\(\left(\frac{x}{365}-a\right)\)___\(\left(\frac{x}{365}-a\right)\)
Qua 2 pứ thì NaCl thu được
\(m_{NaCl}=58,5\left(a+\frac{x}{365}-a\right)=17,55\Rightarrow x=109,5\left(g\right)\)
Thay x tìm được vào (A) và giải:
\(\Rightarrow a=0,1\left(mol\right)\Rightarrow m_{NaOH}=40a=40.0,1=4\left(g\right)\)
À, còn TH A là \(Na_2O\) nữa :v Chia 2 TH và làm tương tự TH2 nhé!