Khi xác định công thức phân tử của một hidrocacbon X trong hai mẫu thí nghiệm, người ta thu được kết quả như sau:
- Đốt cháy hoàn toàn 2,2 gam chất trong mẫu (1), thu được 3,36 lít (đktc) khí CO2.
- Chất trong mẫu (2) có tỉ khối đối với H2 là 22.
Xác định công thức phân tử của X và viết công thức cấu tạo có thể có của X .


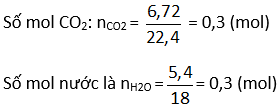
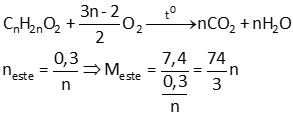
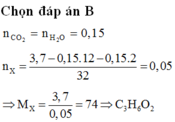
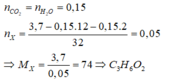

nC = nCO2 = 0,15 (mol); nH = 2nH2O = 2.0,2 = 0,4 (mol)
mC + mH = 0,15.12 + 0.4.2 = 2,2 gam => không có O
nC : nH = 0,15 : 0,4 = 3 : 8
Mà M = 22.2 = 44 => CTPT là C3H8
Vì C3H8 chỉ có một công thức cấu tạo nên kết luận của phòng thí nghiệm là đúng.
Chị ơi cho em hỏi làm sao tính ra số mol của H2O vậy ạ?