Câu 3 : Đốt cháy một hỗn hợp bột Fe và Mg, trong đó Mg có khối lượng là 0,48 gam cần
dùng hết 672 ml O 2 ( đktc).
a) Tính khối lượng sắt và khối lượng hỗn hợp ban đầu ?
b) Tính thành phần phần trăm về khối lượng mỗi chất trong hỗn hợp ban đầu ?
c) Tính khối lượng mỗi oxit thu được sau phản ứng ?
Giups mình với nhé ai nhanh thì mình tick và kết bạn nhé

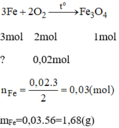
a,đổi.672ml=0,672l
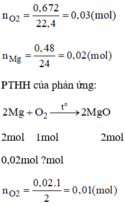
tổng.số.mol.O2.cần.dùng.là:n=V/22,4=0,672/22,4=0,03(mol)
(1)3Fe+2O2--->Fe3O4
(2)2Mg+O2--->2MgO
số.mol.Mg.dùng.trong.PƯ.là:n=m/M=0,48/24=0,02(mol)
theo.PT(.2,)số.mol.O2.cần.dùng.để.tham.gia.PƯ.là:0,02x1:2=0,01(mol)
=>số.mol.O2.dùng.cho.PƯ.(1).là:0,03-0,01=0,02(mol)
theo.PT.(1),số.mol.Fe.là:0,02x3:2=0,03(mol)
Khối.lượng.sắt.là:0,03x56=1,68(g)
khối.lượng.hỗn.hợp.ban.đầu.là.:0,48+1,68=2,16(g)
b,%Fe=1,68x100/2,16=77,(7)%
=>%Mg=100%-77,(7)%=22,(2)%