Cho đinh sắt vào 500ml dd CuSo4. Sau khi phản ứng kết thúc, lấy đinh sắt ra ,rửa nhẹ, cân lại thấy khối lượng đinh sắt tăng 1,6 gam. Biết rằng toàn bộ kim loại tạo thành đều bám vào đinh sắt . a) Viết PTPƯ xảy ra. b) Tính khối lượng sắt tan ra
c) tính Cm của dd CuSo4 dùng trong thí nghiệm trên


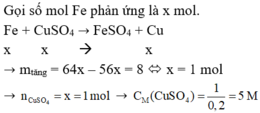
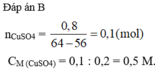
a. \(PTHH:Fe+CuSO_4\rightarrow FeSO_4+Cu\)
b. Gọi số mol Fe phản ứng là a
\(Fe+CuSO_4\rightarrow FeSO_4+Cu\)
a_______a________a _______ a
Gọi khối lượng đinh sắt ban đầu là m
Ta có khối lượng đinh sắt sau phản ứng là
\(m-56a+64a=m+8a\)
Khối lượng tăng 1,6g
\(\rightarrow m+8a-m=1,6\)
\(\rightarrow a=0,2\)
\(\rightarrow m_{Fe_{tan.ra}}=0,2.56=11,2\left(g\right)\)
c. \(CM_{CuSO_4}=\frac{0,2}{0,5}=0,4M\)
a) Fe+CuSO4--->FeSO4+Cu
b) Gọi n Fe tan ra là x--->m Fe=56x
Theo pthh
n Cu=n Fe=x(mol)--->m Cu=64x(g)
Khối lượng sắt sau pư tắng 1,6g
--->64x-56x=1,6
-->8x=1,6
---->x=0,2
m Fe=0,2.56=11,2(g)
c) Theo pthh
n CuSO4=n Fe=0,2(mol)
CM CuSO4=0,2/0,5=0,4(M)