Cho 20g hỗn hợp X gồm zn fe cu vào dd Hcl dư đến khi pư xảy ra hoàn toàn thu được dd Y;5.6 lít khỉ ở đktc và còn lại 5,1 g chất rắn Z
a,viết các pt pư xảy ra
b,tính % kluong mỗi kloai trong hỗn hợp X
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Hai muối tạo ra phải là muối của kim loại mạnh Zn và Fe
Hai kim loại tạo ra phải 1à 2 kim 1oại yếu 1à Ag và Fe => Fe dư => Muối thu được là muối Fe(NO3)2
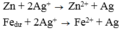

nHCl = nCl- = 2nO = (23,2 - 16,8).2 : 18 = 0,8-> V = 400ml
=> Đáp án A

\(m_{H_2} = m -(m-2,4) = 2,4(gam)\\ \Rightarrow n_{H_2} = \dfrac{2,4}{2} = 1,2(mol)\\ Gọi : n_{Mg} = a ;n_{Zn} = 2a;n_{Fe}= 3a(mol)\\ Mg + 2HCl \to MgCl_2 + H_2\\ Zn + 2HCl \to ZnCl_2 + H_2\\ Fe + 2HCl \to FeCl_2 + H_2\\ n_{H_2} = n_{Mg} + n_{Zn} + n_{Fe} = a + 2a + 3a = 1,2(mol)\\ \Rightarrow a = 0,2;\\ \Rightarrow m = 0,2.24 + 0,2.2.65 + 0,2.3.56 = 64,4(gam)\)
Bạn ơi, kết quả này có chắc là đúng ko? mik có tìm trên gg r mà nó ra kết quả khác

Gọi x, 2x, 3x tương ứng là số mol của Mg, Zn và Fe: 24x + 65.2x + 56.3x = m ---> m = 322x.
Khối lượng dd tăng = khối lượng kim loại - mH2
m - 2,4 = m - (2x + 4x + 9x) ---> 15x = 2,4 hay x = 0,16 mol.
Thay vào trên thu được: m = 322.0,16 = 51,52 gam.
m - 2,4 = m - (2x + 4x + 9x) ---> 15x = 2,4 hay x = 0,16 mol.
Đoạn này mk chưa hiểu lắm
Giảng lại hộ mk vs

a) PTHH: 2Al + 6 HCl -> 2 AlCl3 + 3 H2
x___________3x______________1,5x(mol)
Fe +2 HCl -> FeCl2 + H2
y___2y____y______y(mol)
b) Ta có: m(rắn)= mCu=0,4(g)
=> m(Al, Fe)=1,5-mCu=1,5-0,4=1,1(g)
nH2= 0,04(mol)
Ta lập hpt:
\(\left\{{}\begin{matrix}27x+56y=1,1\\1,5x+y=0,04\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,02\\y=0,01\end{matrix}\right.\)
=> mAl=27.0,02=0,54(g)
mFe=56.0,01=0,56(g)
a) Zn+2HCl---.ZnCl2 +H2
x-----------------------------x
Fe+2HCl--->FeCl2 +H2
y---------------------------y
b) m\(_{Cu}=\)5,1(g)
=>m \(_{Fe+Zn}=20-5,1=14,9\left(g\right)\)
n\(_{H2}=\frac{5,6}{22,4}=0,25\left(mol\right)\)
Suy ra ta có hệ pt
\(\left\{{}\begin{matrix}65x+56y=14,9\\x+y=0,25\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}0,1\\0,15\end{matrix}\right.\)
%m\(_{Cu}=\frac{5,1}{20}.100\%=25,5\%\)
%m\(_{Zn}=\frac{0,1.65}{20}.100\%=32,5\%\)
%m\(_{Fe}=\frac{0,15.56}{20}.100\%=42\%\)