Lấy 10,3g gam hỗn hợp gồm Al và Mg trong dung dịch H2SO4 loãng dư thu được 11,2 lít khí H2 (đktc) tính khối lượng muối sunfat tạo thành 9 (áp dụng định luật bảo toàn khối lượng)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án D
Số mol H2 thu được là : n H 2 = 11 , 2 22 , 4 = 0 , 5 mol
Gọi M là kim loại chung cho Al và Mg với hóa trị n
Sơ dồ phản ứng :
M ⏟ 10 , 2 gam + H 2 S O 4 ( l o ã n g , d ư ) → M 2 ( S O 4 ) n ⏟ m u ố i + H 2 ↑ ⏟ 0 , 5 m o l
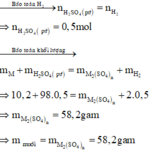

Giả sử: \(\left\{{}\begin{matrix}n_{Al}=x\left(mol\right)\\n_{Fe}=y\left(mol\right)\end{matrix}\right.\)
⇒ 27x + 56y = 11 (1)
Ta có: \(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Theo ĐLBT mol e, có: 3x + 2y = 0,4.2 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,2\left(mol\right)\\y=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Al}=0,2.27=5,4\left(g\right)\\m_{Fe}=0,1.56=5,6\left(g\right)\end{matrix}\right.\)
Bạn tham khảo nhé!

Đáp án B
Ta thấy các kim loại đều phản ứng với axit theo phản ứng tổng quát: R + H2SO4 → RSO4 + H2
Có: nH2 = 6,72: 22,4 = 0,3 mol => nRSO4 = nH2 = 0,3 mol = nSO4
Bảo toàn nguyên tố: mRSO4 = mR + mSO4 = 14 + 0,3.96 = 42,8g

Đáp án C
2107 gam dung dịch H2SO4 loãng, nồng độ 10% gồ 2,15 mol chất tan H2SO4 và 189,3 gam H2O.
→ kết quả cô cạn dung dịch Y thu được 1922,4 gam H2O là gồm lượng sẵn có trên là lượng sinh ra thêm do phản ứng giữa X + H 2 SO 4 ⇒ lượng sinh thêm là 26,1 gam ⇄ 1,45mol
*Sơ đồ phản ứng:
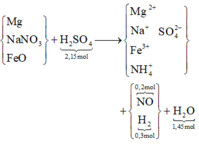
Có sơ đồ, việc giải bài tập trở nên đơn giản, chỉ là thuần “ban bật” bảo toàn nguyên tố qua dấu “ → ”:
Thật vậy, bảo toàn nguyên tố H có 0,2 mol NH 4 + → có 0,4 mol NaNO3 theo bảo toàn nguyên tố N.
Bỏ góc SO4 hai vế rồi bảo toàn nguyên tố O có 0,45 mol
![]()
Mà oxi chiếm 26,4% khối lượng X nên
![]()
Biết lượng FeO, NaNO3 rồi nên suy ra lượng còn lại 33,6 gam là của Mg.
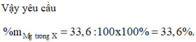

Mg+H2SO4->MgSO4+H2
x-------------------------------x
2Al+3H2SO4->Al2(SO4)3+3H2
y-------------------------------------3\2y
Ta có :
\(\left\{{}\begin{matrix}24x+27y=11,7\\x+\dfrac{3}{2}y=0,6\end{matrix}\right.\)
=>x=0,15 mol , y=0,3 mol
=>m MgSO4=0,15.120=18g
=>m Al2(SO4)3=0,15.342=51,3g



$2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2$
$Mg + H_2SO_4 \to MgSO_4 + H_2$
Theo PTHH :
$n_{H_2SO_4\ pư} = n_{H_2} = \dfrac{11,2}{22,4} = 0,5(mol)$
Bảo toàn khối lượng :
$m_{muối} = 10,3 + 0,5.98 - 0,5.2 = 58,3(gam)$