Người ta trộn 200ml hh khí gồm một hidrocacbon, nito với 450ml khí oxi (lấy dư) rồi đốt cháy hoàn toàn hh thì thu được 700ml hh khí và hơi, làm lạnh hh sản phẩm cho ngưng tụ hết hơi nước thì còn 400ml, sau đó dẫn 400ml còn lại vào kiềm dư thì còn lại 200ml khí. Xác định CTPT của hidrocacbon và % thể tích các khí trong hh ban đầu, các thể tích đo ở cùng đk
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Khi các chất khí đo ở cùng điều kiện thì tỉ lệ mol cũng là tỉ lệ thể tích
TH1: Hai anken

TH2: Hai ankan
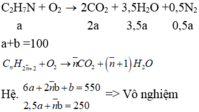

a) PTTH: \(2H_2+O_2\rightarrow2H_2O\)
\(C_2H_2+\dfrac{5}{2}O_2\underrightarrow{t^o}2CO_2+H_2O\)
b) Ta có: \(\left\{{}\begin{matrix}\overline{M}_{hhkhí}=0,5\cdot28=14\\n_{hhkhí}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\end{matrix}\right.\)
Theo phương pháp đường chéo, ta có: \(\dfrac{n_{H_2}}{n_{C_2H_2}}=\dfrac{12}{12}=1\)
\(\Rightarrow n_{H_2}=n_{C_2H_2}=0,3\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{H_2}=\dfrac{0,3}{0,6}\cdot100\%=50\%\\\%V_{C_2H_2}=50\%\\\%m_{H_2}=\dfrac{0,3\cdot2}{5,6}\cdot100\%\approx10,71\%\\\%m_{C_2H_4}=89,29\%\end{matrix}\right.\)

Đổi 10 cm3=10 ml,50cm3=50ml,70cm3=70ml,20cm3=20ml.Sản phẩm sau khi đốt cháy và ngưng tụ hơi nước có thể tích =50ml bao gồm:CO2,O2 dư,sau khi dẫn sản phẩm qua dung dịch kiềm dư thì CO2 được hấp thu vào trong dung dịch kiềm còn 20ml khí thoát ra là thể tích O2 dư=>VCO2 thu được sau khi đốt cháy=50-20=30(ml) và thể tích oxi phản ứng=70-20=50 ml.ta có pt: CxHy +(x+y/4)--->xCO2+y/2 H2O (1)
10ml--------------->x.10ml---->y/2.10ml
lại có VCO2=30=10.x=>x=3,bảo toàn nguyên tố Oxi ta có VO pu=VO(CO2)+VO(H2O)=2.VCO2+VH2O=>VH2O=50.2-30.2=40ml,lại có VH2O=y/2.10=40=>y=8
=> CTPT của X là C3H8.

a,
2H2+ O2 (t*)-> 2H2O
CH4+ 2O2 (t*)-> CO2+ 2H2O
M X= 0,325.32= 10,4
nX= 11,2/22,4= 0,5 mol
Gọi x là nH2, y là nCH4
Ta có 2x+16yx+y=10,42x+16yx+y=10,4
<=> 8,4x= 5,6y
<=> xy=5,68,4=23xy=5,68,4=23
Vậy nếu mol H2 là 2x thì mol CH4 là 3x
=> 2x+ 3x= 0,5 <=> x= 0,1
=> nH2= 0,2 mol; nCH4= 0,3 mol
%H2= 0,2.1000,50,2.1000,5= 40%
%CH4= 60%
b,
nO2= 28,8/32= 0,9 mol
Spu đốt H2, tạo ra 0,2 mol H2O; đã dùng 0,1 mol O2
Spu đôts CH4, tạo ra 0,3 mol CO2; 0,6 mol H2O; đã dùng 0,6 mol O2
=> Dư 0,2 mol O2
Sau khi ngưng tụ nước còn lại hh khí gồm 0,3 mol CO2; 0,2 mol O2
%V CO2= 0,3.1000,3+0,20,3.1000,3+0,2= 60%
%V O2= 40%
mCO2= 0,3.44= 13,2g
mO2= 0,2.32= 6,4g
%m CO2= 13,2.1006,4+13,213,2.1006,4+13,2= 67,3%
%m O2= 32,7%




