1,42g hh CaCO3 và MgCO3 tác dụng với dd HCl dư. Khí bay ra hấp thụ hoàn toàn bằng dd chứa 0,0225 mol Ba(OH)2. Sau phản ứng Ba(OH)2 được tách ra khỏi kết tủa và phản ứng vừa hết với H2SO4 tạo ra 1,7475g muối sunfat kết tủa . Tính khối lượng mỗi chất có trong hh ban đầu
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


CaCO3 + 2HCl--> CaCl2 + H2O + CO2
MgCO3 +2HCl--> MgCl2 + H2O + CO2
CO2 + Ba(OH)2---> BaCO3 + H2O
H2SO4 + Ba(OH)2---> BaSO4 + 2H2O
Ta có nBaSO4=1,7475/233=0,0075 mol = nBa(OH)2 dư
=> nBa(OH)2 PỨ vs CO2= 0,0225-0,0075=0,015 mol = nCO2
Gọi nCaCO3 =x mol ; n MgCO3 = y mol
=> 100x + 84 y= 14,2
và x +y =0,015 mol = nCO2
=> x=0,80875 mol ; y= mình tính ra âm , ko bt có sai đề không

Dẫn khí CO chứ không phải CO2 em nhé
CO + CuO --> Cu + CO2 (1)
hỗn hợp khí thu được gồm \(\left\{{}\begin{matrix}CO_2\\CO_{dư}\end{matrix}\right.\). Cho hỗn hợp khí hấp thụ vào dung dịch Ba(OH)2 thì CO2 sẽ phản ứng
CO2 + Ba(OH)2 --> BaCO3↓ + H2O
nBaCO3 = 59,1/197 = 0,3 mol => nCO2 = 0,3 mol
Theo pư (1) ta thấy nCuO = nCO2 => mCuO = 0,3.80 = 24 gam

\(CaCO_3+2HCl\rightarrow CaCl_2+H_2O+CO_2\uparrow\)
\(x\) \(x\)
\(MgCO_2+2HCl\rightarrow MgCl_2+H_2O+CO_2\uparrow\)
\(y\) \(y\)
Thu đc kết tủa \(BaSO_4\)
\(n_{BaSO_4}=\dfrac{1,7475}{233}=0,0075mol=n_{Ba\left(OH\right)_2dư}\)
\(\Rightarrow n_{Ba\left(OH\right)_2PƯ}=0,0225-0,0075=0,015mol=n_{BaCO_3}\)(BT Ba)
\(\Rightarrow n_{CO_2}=n_{BaCO_3}=0,015mol\left(BtC\right)\)
Ta có:
\(\left\{{}\begin{matrix}100x+84y=1,42\\x+y=n_{CO_2}=0,015\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}x=0,01\\y=0,005\end{matrix}\right.\)
\(m_{CaCO_3}=0,01\cdot100=1g\)
\(m_{MgCO_3}=0,005\cdot84=0,42g\)

Ta có: 100nCaCO3 + 84nMgCO3 = 28,4 (1)
PT: \(CaCO_3+2HCl\rightarrow CaCl_2+CO_2+H_2O\)
\(MgCO_3+2HCl\rightarrow MgCl_2+CO_2+H_2O\)
\(CO_2+Ba\left(OH\right)_2\rightarrow BaCO_3+H_2O\)
Theo PT: nCO2 = nCaCO3 + nMgCO3
nCO2 = nBaCO3
⇒ nCaCO3 + nMgCO3 = nBaCO3
Ta có: \(n_{BaCO_3}=\dfrac{5,91}{197}=0,03\left(mol\right)\)
⇒ nCaCO3 + nMgCO3 = 0,03 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{CaCO_3}=\\n_{MgCO_3}=\end{matrix}\right.\)
Đến đây thì ra số mol âm, bạn xem lại đề nhé.
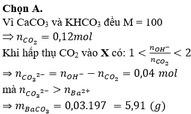
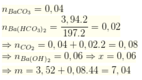
CaCO3+2HCl->CaCl2+CO2+H2O
CO2+Ba[OH]2->BaCO3+H2O
BaOH2 +H2SO4->BaSO4+2H2O
ta co nBaSO4=1,7475:233=0,0075 MOL
=>nBAoh2=nBASO4=0,0075 MOL
nBaOH2 TG PU VOI CO2 =0,0225-0,0075=0,015 mol
->nCO2=0,015 mol
theo pt nCO2=nCaCO3=0,015 mol
mCaCO3=0,015.100=1,5 g
Còn phương trình của MgCO3 với HCl thì sao?