một hỗn hợp khí gồm 32g oxit và 3g hidro. Đốt hỗn hợp khí, phản ứng xong để nguội và cho biết:
a. số phân tử khí nào còn dư, dư bao nhiêu?
b. thể tích của khí dư(đktc) là bao nhiêu?
c. khối lượng của khí dư là bao nhiêu?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{O_2}=\dfrac{32}{32}=1\left(mol\right)\)
\(n_{H_2}=\dfrac{3}{2}=1,5\left(mol\right)\)
1) Vhỗn hợp (đktc) = (1 + 1,5).22,4 = 56 (l)
2) - Số phân tử oxi là: 1.6.1023 = 6.1023 (phân tử)
- Số phân tử hidro là: 1,5.6.1023 = 9.1023 (phân tử)
3) PT: 2H2 + O2 → 2H2O
Trước 1,5 1 0 mol
Trong 1,5 0,75 1,5 mol
Sau 0 0,25 1,5 mol
a) - Oxi dư
- Số phân tử oxi dư là: 0,25.6.1023 = 1,5.1023 = 15.1022 (phân tử)
b) \(V_{O_2dư\left(đktc\right)}=0,25.22,4=5,6\left(l\right)\)
c) \(m_{O_2dư}=0,25.32=8\left(g\right)\)

\(n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(n_{O_2}=\dfrac{8}{22,4}=\dfrac{5}{14}\left(mol\right)\)
PTHH: 2H2 + O2 --to--> 2H2O
Xét tỉ lệ: \(\dfrac{0,5}{2}< \dfrac{\dfrac{5}{14}}{1}\) => H2 hết, O2 dư
PTHH: 2H2 + O2 --to--> 2H2O
0,5-->0,25
=> \(V_{O_2\left(dư\right)}=\left(\dfrac{5}{14}-0,25\right).22,4=2,4\left(l\right)\)

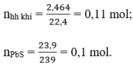
a) Phương trình hóa học của phản ứng:
Fe + 2HCl → FeCl2 + H2 (1)
FeS + 2HCl → FeCl2 + H2S (2)
H2S + Pb(NO3)2 → PbS + 2HNO3 (3)
b) Hỗn hợp khí thu được là H2 và H2S
Theo pt (3) ⇒ nH2S = nPbS = 0,1 mol
⇒ nH2 = nhh khí - nH2S = 0,11 – 0,1 = 0,01 mol
VH2 = 0,01 x 22,4 = 0,224l.
VH2S = 0,1 x 22,4 = 2,24l.
c) Theo PT (2) ⇒ nFeS = nH2S = 0,1 mol
⇒ mFeS = 0,1 × 88 = 8,8g.
Theo PT (1) nFe = nH2 = 0,01 mol ⇒ mFe = 56 × 0,01 = 0,56g.

a)H2+1/2O2--->H2O .theo bài ra và theo pt H2 hết và O2 dư và dư 5ml
b)mH2O=VH2O.dH2O=10gam.
2)a] 2\(H_2\) +\(O_2\) => 2\(H_2O\)
Bđ 10 ml 10 ml
Pứ 10ml=>5ml=>10ml
Dư 5ml
b] Giả sử hiệu suất là 100%
So sánh tỉ lệ thể tích/hệ số pứ của \(H_2\) và \(O_2\)
10/2<10/1 => \(H_2\) pứ hết
Theo pt=>thể tích \(H_2\)dư=5ml= thể tích \(H_2O\) sinh ra
Khối lượng \(H_2O\) =V.D=5g

C2H4+Br2->C2H4Br2
0,05----0,05
n Br2=\(\dfrac{8}{160}\)=0,05 mol
=>%VC2H4=\(\dfrac{0,05.22,4}{5,6}.100=20\%\)
=>%VCH4=80%
c)CH4+2O2-to>CO2+2H2O
1.10-3----2.10-3 mol
C2H4+3O2-to>2CO2+2H2O
2,5.10-4-7,5.10-4 mol
n hh=\(\dfrac{0,028}{22,4}\)=1,25.10-3 mol
=>n C2H4=2,5.10-4 mol
=>n CH4=1.10-3 mol
=>VO2=(2.10-3+7,5.10-4).22,4=0,0616l
\(n_{Br_2}=\dfrac{8}{160}=0,05mol\)
\(\Rightarrow n_{etilen}=n_{Br_2}=0,05mol\)
\(n_{hh}=\dfrac{5,6}{22,4}=0,25mol\)
\(\Rightarrow n_{metan}=n_{hh}-n_{etilen}=0,25-0,05=0,2mol\)
a)\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
b)\(\%V_{metan}=\dfrac{0,2}{0,25}\cdot100\%=80\%\)
\(\%V_{etilen}=100\%-80\%=20\%\)