cho 11 g hỗn hợp Al và Fe vào dd HNO3 loãng dư thì có 6.72 lit(đktc) khí no bay ra.Khối lượng các kim loại Al va Fe trong hỗn hợp đầu lần lượt là?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Theo gt ta có: $n_{NO}=0,3(mol)$
Gọi số mol của Al và Fe trong 11g hỗn hợp lần lượt là a;b(mol)
Ta có: \(\left\{{}\begin{matrix}27a+56b=11\\3a+3b=0,9\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\)
Suy ra $m_{Fe}=5,4(g);m_{Al}=5,6(g)$

Khi không màu hóa nâu trong không khí là NO ( vì NO + O2 --> NO2(màu nâu đỏ).
Al0 --> Al+3 + 3e N+5 +3e --> N+2
Fe0 --> Fe+3 + 3e
nNO =20,16/22,4 = 0,9 mol => số mol e nhận = 0,9.3 = 2,7 mol = ne nhường
Gọi số mol của Al , Fe lần lượt là x và y ta có hệ pt về khối lượng và mol e trao đổi :
\(\left\{{}\begin{matrix}3x+3y=2,7\\27x+56y=38,8\end{matrix}\right.\)=> x = 0,4 mol và y = 0,5 mol
=> mAl = 0,4.27 = 10,8 gam , mFe = 0,5.56 =28 gam

Các quá trình OXH - K
Al0 → Al+3 + 3e N+5 + 3e → N+2
Fe0 → Fe+3 + 3e
nNO = \(\dfrac{3,36}{22,4}\)mol . Gọi số mol của Al va Fe lần lượt là x và y mol ta có hệ:
\(\left\{{}\begin{matrix}27x+56y=5,5\\3x+3y=0,45\end{matrix}\right.\)=> x = 0,1 và y = 0,05 mol
mAl = 0,1.27 = 2,7 gam
mFe = 0,05.56 = 2,8 gam

Đáp án D
Gọi số mol Al, Fe lần lượt là a, b → 27 a + 56 b = 5 , , 5
Bảo toàn e: 3 a + 2 b = 0 , 22
Giải được: a=0,1; b=0,05
Khối lượng Al và Fe lần lượt là 2,7 gam và 2,8 gam

Đáp án D
Do lượng Al trong X và Y như nhau ⇒ khác nhau là do Na, Fe và R
⇒ Bỏ Al ra để tiện xét bài toán ⇒ Xét hỗn hợp X gồm Na, Fe và Y chỉ chứa R.
Giả sử mY = 100g ⇒ ∑mX = 200g.
● Giả sử hỗn hợp X chỉ chứa Na ⇒ nNa = 200 : 23 mol ⇒ nH2 = 100/ 23 mol.
● Giả sử hỗn hợp X chỉ chứa Fe ⇒ nH2 = nFe = 200 : 56 mol = 25 / 7 mol.
Thực tế X chứa cả Na và Fe ⇒ 25 / 7 < nH2 < 100 / 23 mol.
Gọi hóa trị của R là n. Bảo toàn electron: nR = 2nH2 / n.
⇒ 50 / 7n < nR < 200 / 23n ⇒ 11,5n < MR = 100 /nR < 14n.
TH1: n = 1 ⇒ 11,5 < MR < 14 ⇒ không có kim loại nào.
TH2: n = 2 ⇒ 23 < MR < 28 ⇒ R là Magie(Mg) ⇒ chọn D.
TH3: n = 3 ⇒ 34,5 < MR < 42 ⇒ không có kim loại nào.

Chọn đáp án D
Do lượng Al trong X và Y như nhau ⇒ khác nhau là do Na, Fe và R
⇒ bỏ Al ra để tiện xét bài toán ||⇒ xét hỗn hợp X gồm Na, Fe và Y chỉ chứa R.
Giả sử mY = 100g ⇒ ∑mX = 200g.
● Giả sử hỗn hợp X chỉ chứa Na ⇒ nNa = 200 ÷ 23 mol ⇒ nH2 = 100 ÷ 23 mol.
● Giả sử hỗn hợp X chỉ chứa Fe ⇒ nH2 = nFe = 200 ÷ 56 mol = 25 ÷ 7 mol.
► Thực tế X chứa cả Na và Fe ⇒ 25 ÷ 7 < nH2 < 100 ÷ 23 mol.
Gọi hóa trị của R là n. Bảo toàn electron: nR = 2nH2 ÷ n.
⇒ 50 ÷ 7n < nR < 200 ÷ 23n ⇒ 11,5n < MR = 100 ÷ nR < 14n.
TH1: n = 1 ⇒ 11,5 < MR < 14 ⇒ không có kim loại nào.
TH2: n = 2 ⇒ 23 < MR < 28 ⇒ R là Magie(Mg) ⇒ chọn D.
TH3: n = 3 ⇒ 34,5 < MR < 42 ⇒ không có kim loại nào


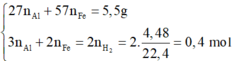
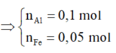
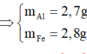
mình chụp bị ngược mất b xem tạm nhé hì hì