dd X gồm MgSO4 và H2SO4. Thêm m (g) Na OH vào 250ml đ X thu được 1,74 g kết tủa và dung dịch Y gồm 2 xation và 1 anion. Cô cạn đ Y thu được 18,78 g chắt rắn khan. Cho 250 ml đ X tác dụng vừa đủ với đ Ba(OH)2 thu được 37,26 g kết tủa. Tính Cm của MgSO4
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Lời giải
n C O 2 sin h r a t r o n g p h ả n ứ n g c ộ n g N a H C O 3 = n C O O H = 0 , 4 ( m o l ) ⇒ n N a t r o n g m u ố i = 0 , 4 ( m o l )
Khi đốt cháy T thu được Na2CO3; CO2 và H2O trong đó ta có:
n C O 2 = n C a C O 3 = 0 , 2 ( m o l ) .
Bảo toàn nguyên tố Na
n N a 2 C O 3 = 1 2 n N a t r o n g m u ố i = 0 , 2 ( m o l )
Bảo toàn nguyên tố C
⇒ n C t r o n g a x i t = n C O 2 ( c h , y ) + n N a 2 C O 3 = 0 , 4 ( m o l )
Đến đây, quan sát các đáp án ta xét 3 trường hợp:
Trường hợp 1: Nếu cả 2 axit đều đơn chức
⇒ n a x i t = n C O O H = 0 , 4 ( m o l ) ⇒ C ¯ a x i t = 1
=>không thỏa mãn
Trường hợp 2: Nếu cả 2 axit đều 2 chức
⇒ n a x i t = n C O O H 2 = 0 , 2 ( m o l ) ⇒ C ¯ a x i t = 2
.Mà cả 2 axit đều 2 chức =>không thỏa mãn
Trường hợp 3: Một axit đơn chức và một axit 2 chức
⇒ n C O O H 2 < n a x i t < n C O O H ⇒ 0 , 2 < n a x i t < 0 , 4 ⇒ 1 < C ¯ a x i t < 2
=> Một axit có 1 nguyên tử C và một axit có 2 nguyên tử C
=>2 axit là HCOOH và (COOH)2
Đáp án A.

Lời giải
n C O 2 = 0 , 4 ( m o l ) ⇒ n - C O O H = n - C O O N a = 0 , 4 ( m o l )
Đốt cháy muối khan ta thu được Na2CO3; CO2 và H2O.
Ta có n N a 2 C O 3 = 1 2 n H C O O N a = 0 , 2 ( m o l ) ; n C O 2 = 0 , 2 ( m o l )
Bảo toàn nguyên tố C n C t r o n g X = 0 , 4 ( m o l ) = n - C O O H
=> 2 axit chỉ có thể là HCOOH và (COOH)2
Đáp án A.

Ta có: nN2 = 0,22 (mol)
⇒ nNO3- = 10nN2 = 2,2 (mol)
⇒ m muối = mX + mNO3- = 31 + 2,2.62 = 167,4 (g)
nHNO3 = 12nN2 = 2,64 (mol)
\(\Rightarrow V_{HNO_3}=\dfrac{2,64}{2}=1,32\left(l\right)=1320\left(ml\right)\)

Đáp án C
Coi dung dịch X thành hỗn hợp Glyxin : 0,2 mol và HCl : x mol
X + KOH : KOH + H2NCH2COOH → H2NCH2COOK + H2O
HCl + KOH → KCl + H2O
→ x = 0,5 – 0,2 = 0,3 → mmuối = 44,95

Đáp án B
nCa = 0,28
nHCl = 2nH2SO4
=>0,28.2 = nHCl + 2nH2SO4 => nHCl = 0,28 => nH2SO4 = 0,14
m+21,14 = 11,2 + 0,14.96 + 0,28.35,5 => m = 13,44g => nO = (13,44 - 21,14)/16 = 0,14
Bảo toàn e : 0,28.2 = 0,14.2 + 8nNH4NO3 + 0,04.3 => nNH4NO3 = 0,02
=>mran khan = 0,28.(40 + 62.2) + 0,02.80 = 47,52g
=>B
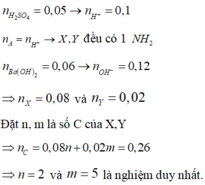
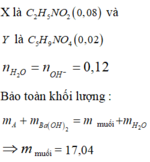
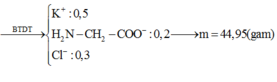

Y chứa 2 cation => Mg2+ chưa kết tủa hết với OH-
nSO42- = nBaSO4; nNa+ = nOH- = 2nMg(OH)2 kt
nNa+ + 2nMg2+ (Y) = 2nSO42- => nMg2+(Y)
=>nMgSO4 = nMg(OH)2 + nMg2+ (Y)
Câu 2 :
X tạo kết tủa với CO2 => X còn có OH- dư
CO2 + 2OH- == > CO32- + H2O
0,3------0,6--------------0,3
CO2 + OH- == > HCO3-
0,1------0,1-------------0,1
=> nCa2+ = nCaCO3 = 0,3 mol
nOH- dư = 0,7 mol
2nCa2+ + nNa+ = nCl- + nOH- dư
mCa2+ + mNa+ + mCl- + mOH- dư = 11,275
=> nNa+ => Nồng độ NaOH trong dung dịch ban đầu