một lượng khí lí tưởng ở điều kiện chuẩn đựng trong một xy lanh được ngăn với bên ngoài bằng một pít tông. Thực hiện giãn nở đẳng áp khối khí. Khi nhiệt độ của khí trong xy lanh là 273*C thì thể tích của khí thay đổi thế nào?
Đáp án: V2 = 2V1
Cần lời giải rõ ràng



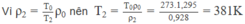
Khí lí tưởng ở điều kiện chuẩn có nhiệt độ \(T_1=0^0C=273K\)
Nhiệt độ lúc sau: \(T_2=273+273=546K\)
Quá trình giãn nở đẳng áp: \(\dfrac{V_1}{T_1}=\dfrac{V_2}{T_2}\Rightarrow \dfrac{V_1}{V_2}=\dfrac{T_1}{T_2}=1/2\)
\(\Rightarrow V_2=2V_1\)
Chúc bạn học tốt