Y là một oxit kim loại chứa 70% kim loại (về khối lượng). Cần dùng bao nhiêu ml dung dịch H2SO4 24,5% (d = 1,2g/ml) để hòa tan vừa đủ 40 gam Y?
K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Những câu hỏi liên quan

MN
4 tháng 8 2019
a.
Ta có :
a + b = 5
M = 27a + Xb = 150
<=> 27a + X ( 5-a ) = 150
<=> 27a + 5X - aX = 150
<=> a( 27 - X ) + 5X = 150
BL :
a = 1 => X = 30.75 (l)
a = 2 => X = 32 (n)
a =3 => X = 34.5 (l)
Vì : a = 2 => b = 3
Vậy: CTHH : Al2S3
b . Gọi: CTHH của oxit : R2On
%R = 2R/(2R+16n) *100% = 70%
<=> 2R + 16n = 20R/7
<=> 16n = 6R/7
<=> R = 56n/3
BL :
n = 3 => R = 56
Vậy: CTHH : Fe2O3
nFe2O3 = 0.25 mol
Fe2O3 + 3H2SO4 --> Fe2(SO4)3 + 3H2O
0.25______0.75
mH2SO4 = 73.5 g
mdd H2SO4 = 300 g
Vdd H2SO4 = 250 ml

23 tháng 12 2017
Giải thích: Đáp án D
nO=0,5nH+=0,04 mol=>mO=0,64 gam=>mM=3,2-0,64=2,56
Giả sử CT oxit là M2On
mM/mO=2M/16n=2,56/0,64=>M=32n
n=2 => M=64 (CuO)
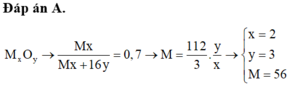
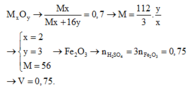
\(CT:A_2O_n\)
\(\%A=\dfrac{2A}{2A+16n}\cdot100\%=70\%\)
\(\Leftrightarrow2A+16n=\dfrac{20}{7}A\)
\(\Leftrightarrow16n=\dfrac{6}{7}A\)
\(\Leftrightarrow A=\dfrac{56}{3}n\)
\(BL:n=3\Rightarrow A=56\)
\(CT:Fe_2O_3\)
\(n_{Fe_2O_3}=\dfrac{40}{160}=0.25\left(mol\right)\)
\(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
\(0.25...........0.75\)
\(m_{dd_{H_2SO_4}}=\dfrac{0.75\cdot98}{24.5\%}=300\left(g\right)\)
\(V_{dd_{H_2SO_4}}=\dfrac{300}{1.2}=250\left(ml\right)\)
Nhận thấy rằng oxit không phải trường hợp đặc biệt $Fe_3O_4$
Nên gọi CTTQ của oxit là $R_2O_x$
Ta có: \(\dfrac{2.R.100\%}{2R+16.x}=70\%\Rightarrow0,6R=11,2x\Rightarrow R=\dfrac{56}{3}x\)
Vậy oxit là $Fe_2O_3$
$Fe_2O_3+3H_2SO_4\rightarrow Fe_2(SO_4)_3+3H_2O$
Ta có: $n_{Fe_2O_3}=0,25(mol)\Rightarrow n_{H_2SO_4}=0,75(mol)\Rightarrow V=250(ml)$