Đổ từ từ 200ml (KHSO4 xM, Na2SO4 0,5M) vào 200 ml (NaHCO3 yM, K2CO3 0,5M ), sau phản ứng thu được 3,36 lít khí (đktc) và dung dịch B. Đổ Ba(OH)2 dư vào B thu được 101,25 gam hỗn hợp kết tủa. Giá trị của x và y là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


n KHSO4 = 0,2x(mol)
n Na2SO4 = 0,2.0,5 = 0,1(mol)
n NaHCO3 = 0,2y(mol)
n K2CO3 = 0,2(mol)
n CO2 = 3,36/22,4 = 0,15(mol)
Bảo toàn nguyên tố với S :
n BaSO4 = n KHSO4 + n Na2SO4 = 0,1 + 0,2x(mol)
Bảo toàn nguyên tố với C :
n BaCO3 + n CO2 = n NaHCO3 + n K2CO3
=> n BaCO3 = 0,2y + 0,05(mol)
Suy ra: (0,1 + 0,2x).233 + (0,2y + 0,05).197 = 134,4(1)
$CO_3^{2-} + H^+ \to HCO_3^-$
$HCO_3^- + H^+ \to CO_2 + H_2O$
Theo PTHH :
n H+ = n KHSO4 = 0,2x = n CO32- + n CO2 = 0,2 + 0,15(2)
Từ (1)(2) suy ra : x = 1,75 ;y =0,5

n NaOH = 0,2x(mol)
n BaCl2 = 0,2(mol)
n NaHCO3 = 0,2y(mol)
n Na2CO3 = 0,1(mol)
n BaCO3 = 29,55/197 = 0,15(mol)
n CO2 = 3,36/22,4 = 0,15(mol)
Bảo toàn nguyên tố với C :
0,2y + 0,1 = 0,15 + 0,15
=> y = 1
Dung dịch A gồm :
Na+ : 0,2x + 0,2y + 0,1 = 0,2x + 0,3(mol)
Ba2+ : 0,2 - 0,15 = 0,05(mol)
Cl- : 0,4(mol)
HCO3- : 0,15(mol)
Bảo toàn điện tích :
0,2x + 0,3 + 0,05.2 = 0,4 + 0,15
=> x = 0,75
anh ơi anh giải thích giúp e dòng HCO3- dưới cái chỗ dd A gồm:

Chọn đáp án D
nH2SO4 = 0,156x0,5 = 0,078 Þ nH+ = 0,078x2 = 0,156
Cho từ từ 0,156 H+ vào

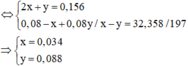
Vậy V = (0,034 + 0,088)x22,4=2,7328

nHCl = 0,5.1,4 = 0,7 (mol) ; nH2SO4 = 0,5.0,5 = 0,25 (mol) => nSO42- = nH2SO4 = 0,25 (mol)
∑ nH+ = nHCl + 2nH2SO4 = 0,7 + 2.0,25 = 1,2 (mol)
nNaOH = 2V (mol) ; nBa(OH)2 = 4V (mol)
∑ nOH- = nNaOH + 2nBa(OH)2 = 2V + 2.4V = 10V (mol)
Các PTHH xảy ra:
H+ + OH- → H2O (1)
Ba2+ + SO42- → BaSO4↓ (2)
Khi cho Zn vào dd C thấy có khí H2 thoát ra => có 2 trường hợp có thể xảy ra. Zn có thể bị hòa tan bởi dung dịch axit hoặc bazo
nH2 = 3,36 : 22,4 = 0,15 (mol)
TH1: dd C có chứa H+ dư => phản ứng (1) OH- phản ứng hết
Zn + 2H+ → Zn2+ + H2↑ (3)
0,3 ← 0,15 (mol)
=> nH+ (1) = ∑ nH+ - nH+ dư = 1,2 – 0,3 = 0,9 (mol)
Theo (1): ∑nOH- = nH+ (1) = 0,9 = 10V => V = 0,09 (lít)
nBa(OH)2 = 4.0,09 = 0,36 => nBa2+ = nBa(OH)2 = 0,36 (mol) > nSO42-
Từ PTHH (2) => nBaSO4 = nSO42- = 0,25 (mol) => mBaSO4 = 0,25.233 = 58,25(g)
TH2: dd C có chứa OH- dư => phản ứng (1) H+ phản ứng hết
Zn + 2OH- → ZnO22- + H2↑ (4)
0,3 ← 0,15 (mol)
=> ∑ nOH- = nOH-(1) + nOH- (4) = 1,2 + 0,3 = 1,5 (mol)
=> 10V = 1,5
=> V = 0,15 (lít)
=> nBa(OH)2 = 0,15. 4 = 0,6 (mol)
=> nBa2+ = 0,6 (mol) > nSO42- = 0,25 (mol)
=> mBaSO4 = 0,25.233 = 58,25 (g)

Đáp án B
► Xét TN1: đặt nCO32– phản ứng = a; nHCO3– phản ứng = b.
⇒ nCO2 = a + b = 0,15 mol; nHCl phản ứng = 2a + b = 0,1875 mol
||⇒ giải hệ có: a = 0,0375 mol; b = 0,1125 mol ⇒ nCO32–/X : nHCO3–/X = a : b = 1 : 3.
► Xét TN2: ∑nC/X = n↓ = 0,25 mol ⇒ 250 ml X chứa 0,5 mol C.
Bảo toàn nguyên tố Cacbon: y = 0,5 – 0,25 = 0,25 mol.
● Chia 0,5 mol C thành 0,125 mol CO32– và 0,375 mol HCO3–.
Bảo toàn điện tích: nK+ = 0,625 mol. Bảo toàn nguyên tố Kali:
x = 0,625 – 0,25 × 2 = 0,125 mol

Đáp án B
► Xét TN1: đặt nCO32– phản ứng = a; nHCO3– phản ứng = b.
⇒ nCO2 = a + b = 0,15 mol; nHCl phản ứng = 2a + b = 0,1875 mol
||⇒ giải hệ có: a = 0,0375 mol; b = 0,1125 mol ⇒ nCO32–/X : nHCO3–/X = a : b = 1 : 3.
► Xét TN2: ∑nC/X = n↓ = 0,25 mol ⇒ 250 ml X chứa 0,5 mol C.
Bảo toàn nguyên tố Cacbon: y = 0,5 – 0,25 = 0,25 mol.
● Chia 0,5 mol C thành 0,125 mol CO32– và 0,375 mol HCO3–.
Bảo toàn điện tích: nK+ = 0,625 mol. Bảo toàn nguyên tố Kali:
x = 0,625 – 0,25 × 2 = 0,125 mol


n KHSO4 = 0,2x(mol)
n Na2SO4 = 0,2.0,5 = 0,1(mol)
n NaHCO3 = 0,2y(mol)
n K2CO3 = 0,1(mol)
n CO2 = 3,36/22,4 = 0,15(mol)
Bảo toàn nguyên tố với S :
n BaSO4 = n KHSO4 + n Na2SO4 = 0,1 + 0,2x(mol)
Bảo toàn nguyên tố với C :
n BaCO3 + n CO2 = n NaHCO3 + n K2CO3
=> n BaCO3 = 0,2y - 0,05(mol)
Suy ra: (0,1 + 0,2x).233 + (0,2y - 0,05).197 = 101,25(1)
$CO_3^{2-} + 2H^+ \to CO_2 + H_2O$
$HCO_3^- + H^+ \to CO_2 + H_2O$
Ta có tỉ lệ :
\(\dfrac{n_{CO_3^{2-}} + n_{HCO_3^-}}{2n_{CO_3^{2-}} + n_{HCO_3^-}} = \dfrac{0,1 + 0,2y}{0,2 + 0,2y} = \dfrac{0,15}{0,2x}\)(2)
Từ (1)(2) suy ra : x = 2,065 ; y <0
=> Sai đề
Phần cuối có thể mình tính toán sai,b tính toán lại nhé