Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
Ta có thành phần chính của quặng: Ca3(PO4)2.
Đặt trong m gam có mCa3(PO4)2 = 0,775m và phần tạp chất có khối lượng tương đương là 0,225m gam
nCa3(PO4)2 = 0,775m/310 = 0,0025m (mol)
Tính độ dinh dưỡng của phân ta quy về P2O5 => nP2O5 = 0,0025m (mol)
Phương trình: Ca3(PO4)2 + 2H2SO4 → Ca(H2PO4)2 + 2CaSO4
0,0025m→ 0,005m (mol)
mSupephotphat đơn = mquặng + mH2SO4 = m + 0,005m.98 = 1,49m (g)
![]()

Theo pt: nNa2HPO4 = 2.nP2O5 = 0,1. 2 = 0,2 mol
Theo định luật bảo toàn khối lượng:
Khối lượng dung dịch sau phản ứng = khối lượng các chất tham gia phản ứng = mNaOH + mP2O5 = 50 + 0,1.142 = 64,2
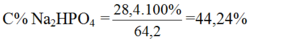

Đáp án A
(a) đúng: anđehit thể hiện tính khử khi tác dụng với O2 hoặc AgNO3/NH3; thể hiện tính oxi hóa khi tác dụng với H2 (xt Ni, t°)
(b) sai. Phenol dễ thế brom hơn benzen (phản ứng điều kiện thường không xúc tác)
(c) đúng: RCHO + H 2 → Ni , t o RCH 2 OH (ancol bậc 1)
(d) đúng: 2CH3COOH + Cu(OH)2 → (CH3COO)2Cu + 2H2O
(e) sai: phenol không làm quỳ tím hóa đỏ (SGK11GB-T92)
(g) đúng: Trong công nghiệp, axeton được sản xuất từ cumen (SGK11CB-192)
Vậy có 4 phát biểu đúng.

Chọn đáp án B
Các phát biểu đúng là: a), c), d), g) => có 4 phát biểu đúng

Chọn đáp án B
Các phát biểu đúng là: a), c), d), g) => có 4 phát biểu đúng

Chọn đáp án B
Các phát biểu đúng là: a), c), d), g) => có 4 phát biểu đúng

- Phát biểu đúng là:
(a) Anđehit vừa có tính oxi hoá vừa có tính khử.
(c) Anđehit tác dụng với H 2 (dư) có xúc tác Ni đun nóng, thu được ancol bậc một.
(d) Dung dịch axit axetic tác dụng được với Cu ( OH ) 2 .
(g) Trong công nghiệp, axeton được sản xuất từ cumen.
- Chọn đáp án A.

Chọn đáp án B
Các phát biểu đúng là: a), c), d), g) => có 4 phát biểu đúng

TH1: Hóa trị `M` đổi `->M:\ Fe`
`Fe^0->Fe^{+2}+2e`
`2H^{-1}+2e->H_2^0`
Bảo toàn electron: `n_{Fe}=n_{H_2}=0,14(mol)`
`->n_{Cu}={11,2-0,14.56}/{64}=0,0525(mol)`
`Cu^0->Cu^{+2}+2e`
`Fe^0->Fe^{+3}+3e`
`S^{+6}+2e->S^{+4}`
Bảo toàn electron: `2n_{Cu}+3n_{Fe}=2n_{SO_2}=0,525`
`->2.0,0525+3.0,14=0,525`
Nhận.
`->M` là Iron `(Fe).`
TH2: Hóa trị `M` không đổi.
`M` hóa trị `n`
Đặt `n_{Cu}=x(mol);n_M=y(mol)`
`M^0->M^{+n}+n.e`
`2H^{-1}+2e->H_2^0`
Bảo toàn electron: `ny=2n_{H_2}=0,28`
`->y={0,28}/n(mol)`
`M^0->M^{+n}+n.e`
`Cu^0->Cu^{+2}+2e`
`S^{+6}+2e->S^{+4}`
Bảo toàn electron: `2x+ny=2n_{SO_2}=0,525`
`->x={0,525-0,28}/2=0,1225(mol)`
`->m_M=11,2-0,1225.64=3,36(g)`
`->M_M={3,36}/{{0,28}/n}=12n`
`->n=2;M_M=24`
`->M` là magnesium `(Mg).`
Vậy `M` là `Mg` hoặc `Fe.`
Đáp án B
Để sản xuất H3PO4 có độ tinh khiết và nồng độ cao hơn, người ta đốt cháy photpho để thu P2O5 rồi cho P2O5 tác dụng với nước
4P + 5O2 → t 0 2P2O5.
P2O5 + 3H2O → 2H3PO4