Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D:
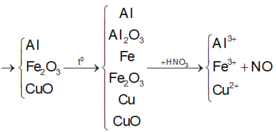
Tóm tắt theo sơ đồ:
rFeoOo t° _ Hòa tan hoàn toàn bằng HNO3

Như vậy, thực chất trong bài toán này chỉ có quá trình cho và nhận electron của nguyên tử Al và N.
Các quá trình nhường và nhận electron như sau:
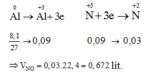

Đáp án B
Trong toàn bộ quá trình chỉ có Al tăng số oxi hóa từ 0 lên +3 và N trong HNO3 giảm số oxi hóa từ +5 xuống +2. Áp dụng định luật bảo toàn mol electron, ta có:
3nAl = 3nNO => nNO = nAl=0,3 => V=6,72 (lít)

Đáp án D
Ta có: nA1 = 0,03 (mol)
Các phương trình phản ứng:
2Al + Fe2O3 → Al2O3 + 2Fe (1)
2Al + 3CuO → Al2O3 + 3Cu (2)
Gọi số mol Al tham gia phản ứng (1) là x, tham gia phản ứng (2) là y.
Theo (1): nFe = nAl = x (mol)
Theo (2): nCu = 3 2 nAl = 3 2 y (mol)
Fe + 4HNO3loãng → Fe(NO3)3 + NO + 2H2O (3)
3Cu + 8HNO3 loãng → 3Cu(NO3)2 + 2NO + 4H2O (4)
Theo (3): nNO/( 3) = nFe = x (mol).
Theo (4): nNO/(4) = 2 3 nCu = 2 3 . 3 2 y = y(mol)
⇒ nNO = x + y = 0,03 (mol) ⇒VNO = 0,03 x 22,4 = 0,672 (lit).

Đáp án C
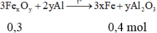
· Phần 2: + NaOH ® 0,015 mol H2
Þ Chứng tỏ phản ứng dư Al, oxit sắt phản ứng hết.
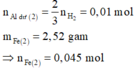
· Phần 1: 14,49 gam Y + HNO3 loãng, dư ® 0,165 mol NO.
Áp dụng bảo toàn electron có:

![]()
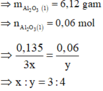
Þ Công thức oxit sắt là Fe3O4.
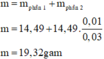

Đáp án B
Nhiệt phân hoàn toàn X ⇒ Y gồm Fe, Al2O3 và Al dư.
Xét phần 2: nAl = nH2 ÷ 1,5 = 0,01 mol; nFe = 0,045 mol
⇒ ne cho TỐI ĐA = 0,01 × 3 + 0,045 × 3 = 0,165 mol.
⇒ phần 1 gấp 0,165 × 3 ÷ 0,165 = 3 lần phần 2.
Xét phần 1: chứa 0,03 mol Al; 0,135 mol Fe.
⇒ nAl2O3 = (14,49 – 0,03 × 27 – 0,135 × 56) ÷ 102 = 0,06 mol.
⇒ nO = 0,18 mol ⇒ x : y = 0,135 ÷ 0,18 = 3 : 4 ⇒ Fe3O4.
m = 4/3 × 14,49 = 19,32(g)

