Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
+ B C P Ư : K ( 0 , 2 m o l ) + H C l ( 0 , 1 m o l ) H 2 O → K + , C l - O H - ⏟ d u n g d ị c h X + H 2 ↑ + B T E : n K = 2 n H 2 B T Đ T c h o X : n K + = n C l - + n O H - ⇒ n H 2 = 0 , 1 n O H - = 0 , 1 ⇒ V H 2 = 2 , 24 l í t m c h ấ t r ắ n = 13 , 05 g a m

Đáp án : B
Xét P1 và P2 : khi số mol HCl tăng thì khối lượng rắn tăng => ở P1 HCl thiếu
=> mrắn – mP1 = mCl pứ => nCl pứ = 0,5 mol = nHCl = 0,5a
=> a = 1 M
Gọi số mol Zn , Mg , Fe trong mỗi phần lần lượt là x , y , z
+) P2 : mrắn – mP2 = mCl pứ => nCl pứ = 0,7 mol < nHCl => kim loại phản ứng hết
=> 2x + 2y + 2z = 0,7 mol
+) P3 : nAg = 2nZn + 2nMg + nFe => 2x + 2y + 3z = 0,8 mol
,mmỗi P = 65x + 24y + 56z = 15,7g
=> x = z = 0,1 ; y = 0,15 mol
=> %nMg = 42,86%

Chọn đáp án A
C H 3 C O O C 6 H 5 + 2 K O H → C H 3 C O O K + C 6 H 5 O K + H 2 O
Có n K O H > n C H 3 C O O C 6 H 5
→ n H 2 O = n C H 3 C O O C 6 H 5 = 0 , 1 m o l
Bảo toàn khối lượng
→ m = 13,6+0,3.56-0,1.18
= 28,6 gam

Đáp án A
Khối lượng chất rắn tăng = mCl đi vào muối
Vì khi tăng HCl thì khối lượng chất rắn tăng => thí nghiệm đầu chắc chắn kim loại dư
=> 34,575 – 18,6 = 35,5.0,5x => x = 0,9
=> nCl muối sau = 0,6 mol < nHCl sau = 0,72 mol => HCl dư
=> nFe + nZn = ½ nCl muối = 0,3 mol và 56nFe + 65nZn = 18,6g
=> nFe = 0,1 => mFe = 5,6g
=>A


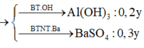
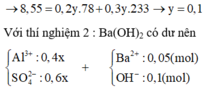

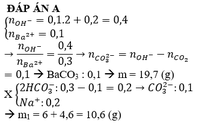

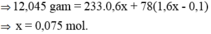
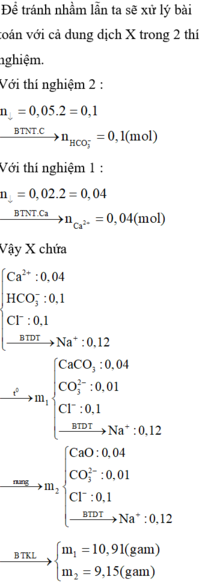
Đáp án D