Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án C
● Gọi số mol NaOH dùng ở lần 1 là a mol ta có sơ đồ.
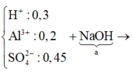
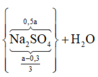
● ⇒ Với nNaOH = (a + 0,45) mol thì nAl(OH)3 = a - 0 , 3 6
+ Ta có sơ đồ:

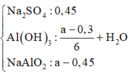
⇒ Ta có nAl(OH)3 = 4nAl(OH)3 – (nNaOH – nH+)
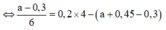
a = 0,6 mol ⇒ VNaOH = 0,6 lít = 600 ml ⇒ Chọn C

Đáp án B
nBa = nBa(OH)2 = 0,3 mol
nSO4 = nH2SO4 + nZnSO4 = 0,325 mol
nOH = 0,8 mol ; nH+ = 0,25 mol ; nZn2+ = 0,2 mol
Ba2+ + SO42- → BaSO4
0,3 → 0,3 mol
nOH (pứ Zn2+) = 0,8 – nH+ = 0,55 mol
=> nOH : nZn2+ = 2,75 => Kết tủa hòa tan 1 phần
=> nZn(OH)2 = 2 nZn2+ – 0,5 nOH = 0,125 mol
=> m = 82,275g

Chọn đáp án B
● Ta có: nBa2+ = 0,3 mol và ∑nSO42– = 0,35 mol.
⇒ nBaSO4 = 0,3 mol ⇒ mBaSO4 = 0,3 × 233 = 69,9 gam.
● Ta có ∑nOH– = 0,8 mol. và nZn2+ = 0,25 mol.
⇒ nZn(OH)2 = 4nZn2+ – ∑nOH– = 0,2 mol.
⇒ mZn(OH)2 = 0,2 × 99 = 19,8 gam.
⇒ Tổng khối lượng kết tủa = 69,9 + 19,8 = 89,7 gam

Đáp án C
0 , 1 m o l F e S O 4 + K M n O 4 0 , 02 m o l H 2 S O 4 0 , 5 m o l → d d X d d X + B a O H 2 → B a S O 4 F e O H 3 M n O H 2
5Fe2+ + MnO4- + 8H+ → 5Fe3+ + Mn2+ + 4H2O
→ nFe3+ = 0,1 mol; ∑nSO42- = 0,1 + 0,5 = 0,6 mol; nMn2+ = 0,02 mol.
m↓ = mFe(OH)3 + mBaSO4 + mMn(OH)2 = 0,1 × 107 + 0,6 × 233 + 0,02 × 89 = 152,28 gam

Đáp án C
Xét hỗn hợp X có tỷ khối hơi so với H2 bằng 17,67 → n(NO) = n(NO2) = z (mol)
Trong hỗn hợp X gọi số mol FeO = x mol; Fe3O4 = y mol → 72x + 232 y = 33,2 gam (1)
Trong dung dịch Y có: Fe3+: x + 3y (mol); H+; K+ (1,2 mol); SO42- (1,2 mol) và NO3- (06 – 3z mol)
Xét phần I:
PTHH: H+ + OH- → H2O; Fe3+ + 3OH- → Fe(OH)3 (0,1 mol)
→ n(H+ dư) = 0,45 – 0,1*3 = 0,15 mol → n(H+ trong Y) = 0,3 mol
Áp dụng ĐLBT số mol e: (2) x + y = 2z*3 + z
Áp dụng ĐLBT điện tích: 3(x + 3y) + 0,3 + 1,2 = 1,2*2 + 0,6 – 3z
Giải (1) (2) (3) → x = 0,3; y = 0,05; z = 0,05

Chọn đáp án C
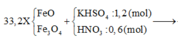
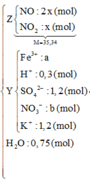
Dùng quy tắc đường chéo => nNO : nN2O = 2 : 1
Gọi số mol của NO và của N2O lần lượt là 2x và x (mol)
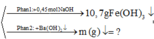
Phần 1: tác dụng với 0,45 mol NaOH → 0,1 mol Fe(OH)3
=> nOH- dùng để trung hòa H+ dư = 0,45 – 3nFe(OH)3 = 0,45 – 0,3 = 0,15 (mol)
=> nH+ dư = 0,15.2 = 0,3 (mol)
Ta có: ∑nH+ bđ = nKHSO4 + nHNO3 = 1,2 + 0,6 = 1,8 (mol)
BTNT H : => nH+ bđ = nH+ dư + 2nH2O => nH2O = ( 1,8 – 0,3)/2 = 0,75 (mol)
BTNT N : 0,6 = 2x + x + b
=> 3x + b = 0,6 (1)
BTĐT đối với các chất trong dd Y: 3a + 0,3+ 1,2 = 2.1,2 + b
=> 3a – b = 0,9 (2)
BTKL: mX + mKHSO4 + mHNO3 = mY + mZ + mH2O
=> 33,2 + 1,2. 136 + 0,6.63 = (56a+ 0,3+1,2.96 +62b+1,2.39) + ( 2x.30 + 46x) + 0,75.18
=> 56a+ 62b+106x=58, 4( 3)
Từ (1), (2), (3) => a= 0,45 ; b= 0,45; x = 0,05 (mol)
Phần 2: Tác dụng với Ba(OH)2 dư
=> m↓ = mBaSO4 + mFe(OH)3 = 0,6.233 + 0,225.107 = 163,875 (g) ( Bảo toàn nguyên tố SO4 và Fe)
Dùng quy tắc đường chéo => nNO : nN2O = 2 : 1
Gọi số mol của NO và của N2O lần lượt là 2x và x (mol)
Phần 1: tác dụng với 0,45 mol NaOH → 0,1 mol Fe(OH)3
=> nOH- dùng để trung hòa H+ dư = 0,45 – 3nFe(OH)3 = 0,45 – 0,3 = 0,15 (mol)
=> nH+ dư = 0,15.2 = 0,3 (mol)
Ta có: ∑nH+ bđ = nKHSO4 + nHNO3 = 1,2 + 0,6 = 1,8 (mol)
BTNT H : => nH+ bđ = nH+ dư + 2nH2O => nH2O = ( 1,8 – 0,3)/2 = 0,75 (mol)
BTNT N : 0,6 = 2x + x + b
=> 3x + b = 0,6 (1)
BTĐT đối với các chất trong dd Y: 3a + 0,3+ 1,2 = 2.1,2 + b
=> 3a – b = 0,9 (2)
BTKL: mX + mKHSO4 + mHNO3 = mY + mZ + mH2O
=> 33,2 + 1,2. 136 + 0,6.63 = (56a+ 0,3+1,2.96 +62b+1,2.39) + ( 2x.30 + 46x) + 0,75.18
=> 56a+ 62b+106x=58, 4( 3)
Từ (1), (2), (3) => a= 0,45 ; b= 0,45; x = 0,05 (mol)
Phần 2: Tác dụng với Ba(OH)2 dư
=> m↓ = mBaSO4 + mFe(OH)3 = 0,6.233 + 0,225.107 = 163,875 (g) ( Bảo toàn nguyên tố SO4 và Fe)

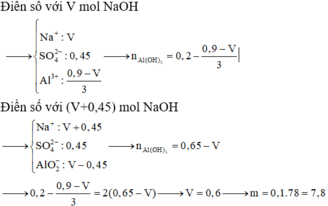
Đáp án D
Định hướng tư duy giải