Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta thấy khi cho Br 2 vào dung dịch 2 muối S 4 + thì toàn bộ S 4 + sẽ bị oxi hoá lên S 6 + ( SO 4 2 - )do đó :
n SO 2 = n SO 4 2 - = 0,15
=> m BaSO 4 = 0,15.233 = 34,95g

Đáp án B
Vì H2SO4 đặc nóng dư nên khí A sinh ra là SO2.
Muối khan thu được là
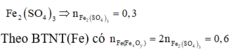
Vì dung dịch NaOH dư nên khỉ dẫn SO2 vào đung dịch NaOH chỉ xảy ra một phản ứng:
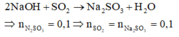
Coi oxit FexOy ban đầu là hỗn hợp của Fe và O.
Gọi nO = a.
Áp dụng định luật bảo toàn moi electron, ta có:


nNa+ = 0,016 mol
Gọi số mol của Cl- và SO42- lần lượt là a, b
Bảo toàn điện tích: a + 2b = 0,016 (1)
Từ khối lượng muối: 35,5a + 96b = 1,036 - 0,016.23 = 0,668 (2)
Từ (1), (2) suy ra: nCl- = 0,008 mol ; nSO42- = 0,004 mol
=> CmHCl = 0,8 M ; CmH2SO4 = 0,4 M

1)
- TN1:
\(n_{AgCl}=\dfrac{35,875}{143,5}=0,25\left(mol\right)\)
PTHH: AgNO3 + HCl --> AgCl + HNO3
0,25<--0,25
TN2:
nNaOH = 0,5.0,3 = 0,15 (mol)
PTHH: NaOH + HCl --> NaCl + H2O
0,15--->0,15
\(n_{HCl\left(dd.C\right)}=0,25+0,15\) = 0,4 (mol)
=> \(C_{M\left(dd.C\right)}=\dfrac{0,4}{2}=0,2M\)
2)
Có \(\left\{{}\begin{matrix}C_{M\left(A\right)}=\dfrac{0,25}{V}M\\C_{M\left(B\right)}=\dfrac{0,15}{V^,}M\end{matrix}\right.\)
nHCl(A) = \(\dfrac{0,025}{V}\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
\(\dfrac{0,025}{V}\)------>\(\dfrac{0,0125}{V}\)
nHCl(B) = \(\dfrac{0,015}{V^,}\) (mol)
PTHH: Fe + 2HCl --> FeCl2 + H2
\(\dfrac{0,015}{V^,}\)-------->\(\dfrac{0,0075}{V^,}\)
TH1: \(\dfrac{0,0125}{V}=\dfrac{0,0075}{V^,}+0,02\)
Mà V + V' = 2 (l)
=> \(\left[{}\begin{matrix}V=1,5;V^,=0,5\left(KTM\right)\\V=0,5;V^,=1,5\left(TM\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}C_{M\left(A\right)}=\dfrac{0,25}{0,5}=0,5M\\C_{M\left(B\right)}=\dfrac{0,15}{1,5}=0,1M\end{matrix}\right.\)
TH2: \(\dfrac{0,0125}{V}+0,02=\dfrac{0,0075}{V^,}\)
=> \(\left[{}\begin{matrix}V=\dfrac{1+\sqrt{6}}{2};V^,=\dfrac{3-\sqrt{6}}{2}\\V=\dfrac{1-\sqrt{6}}{2}\left(L\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}C_{M\left(A\right)}=\dfrac{0,25}{\dfrac{1+\sqrt{6}}{2}}=\dfrac{-1+\sqrt{6}}{10}M\\C_{M\left(B\right)}=\dfrac{0,15}{\dfrac{3-\sqrt{6}}{2}}=\dfrac{3+\sqrt{6}}{10}M\end{matrix}\right.\)

- PT: a, \(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\) (1)
\(MnO_2+4HCl_đ\underrightarrow{t^o}MnCl_2+Cl_2+2H_2O\) (2)
- Ta có: \(n_{HCl\left(1\right)}=n_{HCl\left(2\right)}=0,2.2=0,4\left(mol\right)\)
Theo PT (1): \(n_{Cl_2}=\dfrac{5}{16}n_{HCl\left(1\right)}=0,125\left(mol\right)\Rightarrow V_1=0,125.22,4=2,8\left(l\right)\)
(2): \(n_{Cl_2\left(2\right)}=\dfrac{1}{4}n_{HCl\left(2\right)}=0,1\left(mol\right)\Rightarrow V_2=0,1.22,4=2,24\left(l\right)\)

a)2Al+6HCl→2AlCl3+3H2
Fe+2HCl→FeCl2+H2
2Al+6H2SO4→Al2(SO4)3+3SO2+6H2O
2Fe+6H2SO4→Fe2(SO4)3+3SO2+6H2O
Cu+2H2SO4→CuSO4+SO2+2H2O
hh:Al(amol),Fe(bmol),Cu(cmol)
nNaOH=0,2×2=0,4mol
nHCl=0,4×2=0,8mol
⇒nHClpu=0,8−0,4=0,4mol
nSO2=5,6\22,4=0,25mol
27a+56b+64c=14,2
0,5a×3+0,5b×2=0,4
0,5a×1,5+0,5b×1,5+0,5c=0,25
⇒a=0,2;b=0,1;c=0,05
mAl=0,2×27=5,4g
mFe=0,1×56=5,6g
mCu=0,05×64=3,2g
b)mddspu=7,1+50−0,25×64=41,1g
C%Al2(SO4)3=41,6%
C%Fe2(SO4)3=24,33%
C%CuSO4=9,73%



Các pthh xảy ra:
\(NaOH+HCl\rightarrow NaCl+H_2O\)
\(NaOH+HNO_3\rightarrow NaNO_3+H_2O\)
\(2NaOH+H_2SO_4\rightarrow Na_2SO_4+H_2O\)
Cho B tác dụng với \(BaCl_2dư\) chỉ có \(H_2SO_4\) phản ứng.
\(BaCl_2+H_2SO_4\rightarrow BaSO_4\downarrow+2HCl\)