Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Tham khảo:
- Trích mẫu thử.
Cho lần lượt vào mỗi mẫu thử một mẩu giấy quỳ tím.
+ Giấy quỳ tím chuyển sang màu đỏ → mẫu thử là acetic acid và acrylic acid (nhóm I);
+ Giấy quỳ tím không đổi màu → mẫu thử là ethanol và acetaldehyde (nhóm II). Phân biệt nhóm I: Dùng dung dịch bromine
+ Dung dịch bromine nhạt dần đến mất màu → mẫu thử là acrylic acid.
CH2 = CH – COOH + Br2 → CH2Br – CHBr – COOH.
+ Dung dịch bromine không bị mất màu → mẫu thử là acetic acid.
Phân biệt nhóm II: Dùng dung dịch bromine
+ Dung dịch bromine nhạt dần đến mất màu → mẫu thử là acetaldehyde CH3CHO + Br2 + H2O → CH3COOH + 2HBr.
+ Dung dịch bromine không bị mất màu → mẫu thử là ethanol.

Tham khảo
- Đánh số thứ tự cho từng dung dịch. Trích dung dịch làm mẫu thử đánh số thứ tự tương ứng.
- Nhúng mẩu quỳ tím vào các mẫu thử:
+ Mẫu thử chứa acetic acid làm quỳ tím hóa đỏ.
+ Ba mẫu thử chứa ethanol, glycerol, acetaldehyde không làm quỳ tím đổi màu.
- Tiếp tục trích mẫu thử của ba dung dịch không làm quỳ tím đổi màu.
- Cho vào mỗi mẫu thử vài giọt dung dịch copper(II) sulfate và 1 mL dung dịch sodium hydroxide, tạo kết tủa xanh lam Cu(OH)2.
CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4
- Lắc nhẹ các mẫu thử:
+ Mẫu thử chứa glycerol làm tan kết tủa xanh lam thành dung dịch màu xanh lam.
+ Hai mẫu thử chứa ethanol và acetaldehyde không làm tan kết tủa.
- Tiếp tục đun nóng nhẹ hai mẫu thử chứa ethanol và acetaldehyde và Cu(OH)2:
+ Mẫu thử chứa acetaldehyde xuất hiện kết tủa đỏ gạch Cu2O.
CH3CHO + 2Cu(OH)2 + NaOH CH3COONa + Cu2O + 3H2O
+ Mẫu thử không có hiện tượng là ethanol.

\({\rm{C}}{{\rm{H}}_{\rm{3}}}\mathop {\rm{C}}\limits^{ + 1} {\rm{H = O + }}{\mathop {{\rm{Br}}}\limits^0 _{\rm{2}}}{\rm{ + }}{{\rm{H}}_{\rm{2}}}{\rm{O}} \to {\rm{C}}{{\rm{H}}_{\rm{3}}}\mathop {\rm{C}}\limits^{ + 3} {\rm{OOH + 2H}}\mathop {{\rm{Br}}}\limits^{ - 1} \)
Trong phản ứng trên, số oxi hoá của C (trong nhóm chức –CHO) tăng từ +1 lên +3, CH3CHO là chất oxi hóa. Số oxi hóa của Br giảm từ 0 xuống -1 , Br2 là chất oxi hóa.

Hiện tượng: Phản ứng sinh ra chất lỏng, nhẹ hơn nước, có mùi thơm đặc trưng.
Giải thích bằng phương trình hoá học:
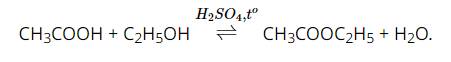

Tham khảo:
1. Quỳ tím chuyển sang màu đỏ vì acetic acid có tính acid.
2. Kim loại tan dần tạo thành dung dịch màu không màu và có khí không màu thoát ra.
- Mg + 2CH3COOH → (CH3COO)2Mg + H2
3. Tạo dung dịch không màu và có khí thoát ra.
- 2CH3COOH + Na2CO3 → 2CH3COONa + CO2 + H2O

\({{\rm{n}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOH}}}}{\rm{ = }}\frac{{\rm{6}}}{{{\rm{60}}}}{\rm{ = 0,1 (mol); }}{{\rm{n}}_{{{\rm{C}}_2}{{\rm{H}}_5}{\rm{OH}}}}{\rm{ = }}\frac{{{\rm{5,2}}}}{{46}}{\rm{ }} \approx {\rm{ 0,113 (mol)}}\)
Phương trình hóa học:
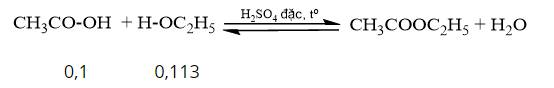
Ta có: \(\frac{{0,1}}{1} < \frac{{0,113}}{1}\) => acetic acid hết, ester tính theo acetic acid.
\(\begin{array}{l}{{\rm{n}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COO}}{{\rm{C}}_2}{{\rm{H}}_5}}}{\rm{ = }}{{\rm{n}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COOH}}}}{\rm{ = 0,1 (mol) }}\\ \Rightarrow {{\rm{m}}_{{\rm{C}}{{\rm{H}}_{\rm{3}}}{\rm{COO}}{{\rm{C}}_2}{{\rm{H}}_5}}} = {\rm{0,1}} \times {\rm{88 = 8,8 (g)}}\\ \Rightarrow {\rm{H = }}\frac{{5,28}}{{8,8}} \times 100\% = 60\% \end{array}\)

- Sử dụng thuốc thử Tollens hoặc Cu(OH)2 trong môi trường kiềm để phân biệt acetaldehyde và acetone
- Lí do sử dụng: acetone không có phản ứng với thuốc thử Tollens hoặc Cu(OH)2 trong môi trường kiềm.

Tham khảo:
- Trong dung dịch nước, chỉ một phần nhỏ carboxylic acid phân li thành ion, vì vậy carboxylic là những acid yếu. Tuy nhiên, chúng thể hiện đầy đủ các tính chất của một acid:
+ Tác dụng với kim loại đứng trước hydrogen trong dãy hoạt động hoá học của kim loại và giải phóng khí hydrogen.
+ Tác dụng được với các base và basic oxide để tạo thành muối và nước.
+ Tác dụng được với một số muối.



Tham khảo
- Đánh số thứ tự cho từng dung dịch. Trích dung dịch làm mẫu thử đánh số thứ tự tương ứng.
- Nhúng mẩu quỳ tím vào các mẫu thử:
+ Mẫu thử chứa acetaldehyde không làm quỳ tím đổi màu.
+ Hai mẫu thử chứa acetic acid, acrylic acid làm quỳ tím hóa đỏ.
- Tiếp tục trích mẫu thử của hai dung dịch làm quỳ tím hóa đỏ.
- Nhỏ vài giọt nước bromine vào hai mẫu thử:
+ Mẫu thử chứa acrylic acid làm nước bromine mất màu.
+ Mẫu thử chứa acetic acid không làm nước bromine mất màu.
* Phương trình hóa học:
CH2=CH–COOH + Br2 → CH2Br – CHBr – COOH