Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
NH4NO2 → N2+ 2H2O
x x 2x mol
mchất rắn giảm= mN2+ mH2O= 28x + 2. 18x= 32-10= 22
→ x= 0,34375 mol
→ H= nNH4NO2 pứ/ nNH4NO2 ban đầu= x/0,5.100%= 68,75%

Chọn đáp án D
NH4NO2![]() N2 + 2H2O
N2 + 2H2O
⇒ nN2 = nNH4NO2 = 0,25 mol
⇒ VN2 = 5,6 lít

Đáp án B
(NH4)2Cr2O7 → Cr2O3+ N2 + 4H2O
x mol x x 4x mol
mchất rắn giảm= mN2+ mH2O= 28x + 18.4x= 32-20
→ x= 0,12 mol; n(NH4)2Cr2O7 ban đầu=8/63 mol
H = npứ/ nban đầu. 100%= 94,5%

Đáp án C
NH4NO2 -> N2 + 2H2O
0,625 -> 0,625 mol
=> VN2 = 14 lit

Đáp án B
Đặt CTPT của X là CxHyOz
Do ở cùng điều kiện nhiệt độ và áp suất thì tỉ lệ về thể tích cũng chính là tỉ lệ về số mol.
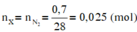
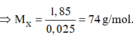

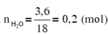
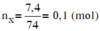
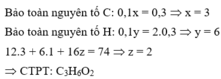

Đáp án C
Hướng dẫn giải:
NH4NO3 → N2O + 2H2O
x x 2x mol
Khối lượng chất rắn giảm chính là do N2O và H2O bay hơi
→mN2O+ mH2O= 44x + 2x.18= 80x = 40-10=30 gam → x= 0,375 mol
→Vkhí và hơi= 3x.22,4=25,2 lít

Đáp án C
Gọi công thức phân tử của X là CxHyNt
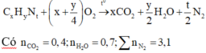
![]()
Mà thể tích trong không khí của O2 và N2 lần lượt là 20% và 80%
![]()
![]()
![]()
![]()
Vì CTĐGN của X cũng là CTPT
Nên CTPT của X là C2H7N

\(n_{NH_4NO_2}=0,1\left(mol\right)\)
Bảo toàn nguyên tố N:
\(2n_{N_2}=2n_{NH_4NO_2}\)
\(\Rightarrow n_{N_2}=n_{NH_4NO_3}=0,1\left(mol\right)\)
\(\Rightarrow V_{N_2}=0,1.22,4=2,24\left(l\right)\)