Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi số mol O2, O3 là a, b (mol)
Có: \(\dfrac{32a+48b}{a+b}=16,2.2=32,4\left(g/mol\right)\)
=> 0,4a = 15,6b
=> a = 39b
\(\%V_{O_3}=\dfrac{b}{a+b}.100\%=\dfrac{b}{39b+b}.100\%=2,5\%\)

Đáp án C.
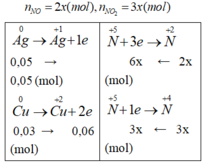
9x = 0,11; x= 11/900 => V = 5x.22,4 = 1,368 (l)

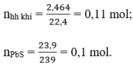
a) Phương trình hóa học của phản ứng:
Fe + 2HCl → FeCl2 + H2 (1)
FeS + 2HCl → FeCl2 + H2S (2)
H2S + Pb(NO3)2 → PbS + 2HNO3 (3)
b) Hỗn hợp khí thu được là H2 và H2S
Theo pt (3) ⇒ nH2S = nPbS = 0,1 mol
⇒ nH2 = nhh khí - nH2S = 0,11 – 0,1 = 0,01 mol
VH2 = 0,01 x 22,4 = 0,224l.
VH2S = 0,1 x 22,4 = 2,24l.
c) Theo PT (2) ⇒ nFeS = nH2S = 0,1 mol
⇒ mFeS = 0,1 × 88 = 8,8g.
Theo PT (1) nFe = nH2 = 0,01 mol ⇒ mFe = 56 × 0,01 = 0,56g.
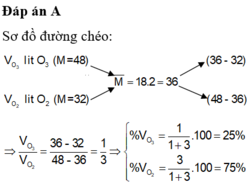
Hỗn hợp khí ozon và oxi có tỉ khối so với khí H 2 là 18. Xác định % thể tích của ozon trong hỗn hợp.

Gọi x là số mol O 3 có trong 1 mol hỗn hợp khí, số mol O 2 sẽ là (1 - x) mol.
Ta có phương trình : 48x + (1 - x).32 = 18.2
Giải ra x = 0,25.
Do %n = %V nên ozon chiếm 25% thể tích hỗn hợp.

Gọi số mol O3, O2 là a, b (mol)
Có: \(M_X=\dfrac{48a+32b}{a+b}=4.10=40\left(g/mol\right)\)
=> a = b (1)
PTHH: 2Ag + O3 --> Ag2O + O2
a------------->a
=> a + b = 0,5 (2)
(1)(2) => a = b = 0,25 (mol)
=> VX = (0,25 + 0,25).22,4 = 11,2 (l)